Титан и его сплавы стали краеугольными материалами для современных дентальных имплантатов благодаря своей превосходной биосовместимости, механическим свойствам и способности к остеоинтеграции. В данной статье систематически описывается классификация титановых материалов, их основные свойства, широкое применение в стоматологии (с акцентом на имплантаты), технологии обработки и их влияние, текущие проблемы и перспективы, такие как новые сплавы, аддитивное производство и наноинженерия поверхности, с целью предоставить теоретические рекомендации для клинической практики и исследований.

1. Введение
Титан (Ti), 22-й элемент в периодической таблице, представляет собой серебристо-белый переходный металл. С 1950-х годов, когда шведский ученый Пер-Ингвар Бронемарк обнаружил, что титан может образовывать прямое, функциональное и структурное соединение с костной тканью (так называемая "остеоинтеграция"), титан открыл блестящую главу в биомедицинской области, особенно в дентальной имплантологии. Его уникальное сочетание свойств идеально соответствует строгим требованиям, предъявляемым к материалам для реабилитации полости рта: отличная биосовместимость, позволяющая избежать отторжения, чрезвычайно высокая удельная прочность, позволяющая выдерживать жевательные нагрузки, исключительная коррозионная стойкость против эрозии слюны и хорошая остеокондуктивность, обеспечивающая долгосрочную стабильность. Успех и предсказуемость лечения с помощью дентальных имплантатов в значительной степени зависят от этих основных характеристик титана, что делает его незаменимым "королем биоматериалов" в реставрации зубов, особенно при восстановлении утраченных зубов.
2. Классификация титана и титановых сплавов
Титановые материалы, используемые в стоматологии, можно разделить на две основные категории в зависимости от их состава и свойств:
- 2.1 Коммерчески чистый титан (CP Ti):
- Согласно стандартам ASTM (например, F67), титан CP подразделяется на классы от 1 до 4 в зависимости от содержания таких межзерновых элементов, как кислород и железо.
- Характеристики: Обладает наилучшей биосовместимостью (наиболее инертен), отличной коррозионной стойкостью и хорошей пластичностью, что облегчает его обработку. Однако его прочность (особенно предел текучести и усталостная прочность) относительно низка.
- Применение в стоматологии: В основном используется для изготовления имплантатов, абатментов, каркасов коронок и мостов, а также ортодонтических брекетов, где требования к прочности не являются экстремальными. Наиболее широко используется CP Ti Grade 4.
- 2.2 Титановые сплавы:
- Добавление легирующих элементов (например, Al, V, Nb, Zr, Mo, Ta) улучшает механические свойства титана.
- Представительский сплав - Ti-6Al-4V (Grade 5):
- Классический титановый сплав с α+β-фазой (алюминий 6% стабилизирует α-фазу, ванадий 4% - β-фазу).
- Характеристики: Значительно прочнее, чем CP Ti (примерно в два раза прочнее CP Ti Grade 4), обладает превосходными усталостными свойствами и хорошей коррозионной стойкостью. Однако существуют опасения по поводу потенциальной биологической токсичности ванадия (V) и алюминия (Al) (несмотря на ограниченные клинические данные), а модуль упругости этого материала все еще выше, чем у кости.
- Другие новые/специфические стоматологические сплавы:
- Ti-6Al-7Nb, Ti-5Al-2.5Fe: Разработана для замены Ti-6Al-4V, без использования ванадия для лучшей биосовместимости.
- Титановые сплавы β-типа (например, Ti-13Nb-13Zr, Ti-12Mo-6Zr-2Fe - TMZF, Ti-35Nb-7Zr-5Ta): В качестве основных легирующих элементов используются ниобий (Nb), тантал (Ta), цирконий (Zr) и молибден (Mo).
- Характеристики: Более низкий модуль упругости (ближе к костной ткани, что снижает экранирование напряжений), более высокая усталостная прочность и вязкость разрушения, отличная коррозионная стойкость, отсутствие спорных элементов (таких как V и Al), а также превосходная биосовместимость. В настоящее время эти вопросы находятся в центре внимания исследователей.
- Сплавы Ti-Zr (например, Roxolid® - Ti-15Zr): Разработан специально для стоматологии, обладает более высокой прочностью, чем CP Ti, и приближается к прочности Ti-6Al-4V, но по биосовместимости приближается к чистому титану и имеет умеренный модуль упругости. Особенно подходит для имплантатов малого диаметра.
Таблица 1: Сравнение свойств распространенного стоматологического титана и титановых сплавов
| Тип материала | Типичный класс | Основной состав | Преимущества | Ограничения | Основные области применения в стоматологии |
|---|---|---|---|---|---|
| Коммерчески чистый титан | 1 класс | >99% Ti | Лучшая биосовместимость, отличная коррозионная стойкость, пластичность | Наименьшая прочность | Тонкостенные части, мембраны |
| 2 класс | >98,9% Ti | Хорошие общие характеристики (баланс биосовместимости, коррозионной стойкости, прочности, пластичности) | Умеренная прочность | Абатменты, небольшие реставрации, скобы | |
| 3 класс | >98,8% Ti | Более высокая прочность по сравнению с классом 2 | Немного менее вязкий, чем Grade 2 | Имплантаты (некоторые), абатменты, каркасы | |
| 4 класс | >98.6% Ti | Самый сильный CP Ti | Более низкая пластичность, чем у низкосортного CP Ti | Основные имплантаты, абатменты, дуги | |
| α+β Титановые сплавы | Ti-6Al-4V (Gr5) | Ti-6Al-4V | Высокая прочность, отличная усталостная прочность | Содержит Al/V (потенциальная биотоксичность), высокий модуль упругости | Имплантаты в зонах повышенной нагрузки, соединители, хирургические инструменты |
| Ti-6Al-7Nb | Ti-6Al-7Nb | Прочность близка к Gr5, нет V (лучшая биосовместимость) | Содержит Al | Имплантаты (заменитель Gr5) | |
| Сплавы β-типа | Ti-13Nb-13Zr | Ti-13Nb-13Zr | Низкий модуль упругости, отличная биосовместимость, отсутствие Al/V | Комплексная обработка | Имплантаты (для смягчения защиты от стресса), ортодонтическая проволока |
| Ti-12Mo-6Zr-2Fe (TMZF) | Ti-12Mo-6Zr-2Fe | Низкий модуль упругости, высокая прочность, хорошая коррозионная стойкость | Содержит Fe (ограниченные долгосрочные биологические данные) | Имплантаты, ортопедические имплантаты | |
| Сплав для стоматологии | Ti-15Zr (Roxolid®) | Ti-15Zr | Значительно прочнее, чем CP4, близко к Gr5, биосовместимость близка к CP Ti | Более высокая стоимость | Имплантаты малого диаметра/узкого гребня |
(Примечание: Данная таблица представляет собой упрощенное сравнение. Точные параметры должны быть указаны в стандартах на материалы и данных производителя. Модуль упругости: CP Ti ~100-110 ГПа, Ti-6Al-4V ~110-115 ГПа, β-сплавы ~55-85 ГПа, кортикальная кость ~10-30 ГПа)
3. Основные преимущества титана в стоматологии
Титан и его сплавы обладают беспрецедентными преимуществами при использовании в стоматологии:
- 3.1 Выдающаяся биосовместимость и устойчивость к коррозии:
- Биосовместимость: Титан может спонтанно образовывать плотную, стабильную и инертную пассивную пленку диоксида титана (TiO₂) в физиологической среде. Эта пленка эффективно изолирует выход ионов металла в окружающие ткани, сводя к минимуму воспаление и иммунное отторжение - необходимое условие для остеоинтеграции. Многочисленные клинические исследования и данные долгосрочного наблюдения подтверждают отличную реакцию тканей на титановые имплантаты.
- Устойчивость к коррозии: Пассивный слой TiO₂ обладает высокой устойчивостью к воздействию жидкостей организма (слюна, кровь, интерстициальная жидкость), фторидов (из зубной пасты и ополаскивателей для полости рта) и колебаний pH полости рта (например, от кислых продуктов и напитков). Даже при длительной эксплуатации такие проблемы, как точечная коррозия, щелевая коррозия или коррозионное растрескивание под напряжением, встречаются крайне редко, что обеспечивает долгосрочную химическую стабильность и безопасность имплантатов в суровой среде полости рта.
- 3.2 Высокое соотношение прочности к весу (высокая удельная прочность):
Титан имеет значительно меньшую плотность (~4,5 г/см³), чем нержавеющая сталь (~8 г/см³) и кобальто-хромовые сплавы (~8,5 г/см³), однако его прочность (особенно титановых сплавов) сопоставима с этими материалами или даже превосходит их. Это означает, что титановые реставрации или имплантаты могут обеспечивать достаточную несущую способность (выдерживать жевательные нагрузки, обычно до нескольких сотен ньютонов) и при этом иметь меньший вес, что снижает нагрузку на опорные ткани и повышает комфорт пациента. - 3.3 Отличная способность к остеоинтеграции:
В этом заключается основное преимущество титана как материала для имплантатов. Слой TiO₂ на поверхности титана является биоактивным и может избирательно адсорбировать белки из крови и жидкостей организма (такие как фибриноген и фибронектин), способствуя адгезии, пролиферации и дифференциации остеобластов. В конечном итоге новая костная ткань может непосредственно откладываться и плотно прилегать к поверхности титана, образуя прямое структурное и функциональное соединение без фиброзного соединительнотканного интерфейса. Такая прямая интеграция кости с имплантатом обеспечивает биологическую основу для долгосрочной стабильной фиксации имплантата. - 3.4 Радиолуценция и эстетические преимущества:
Радиолюценция: Титан обладает гораздо меньшим ослаблением рентгеновского излучения, чем традиционные металлы, такие как сплавы золота и кобальто-хромовые сплавы. На рентгенограммах (периапикальных, панорамных, CBCT) титановые имплантаты выглядят как изображения с относительно низкой плотностью, что позволяет четко визуализировать окружающую костную структуру. Это облегчает врачам точную оценку состояния остеоинтеграции, изменений уровня маргинальной кости и здоровья периимплантата, что делает его ключевым для долгосрочного последующего мониторинга.
Эстетическое преимущество: При тонкой десне или поверхностном расположении имплантатов (особенно в передней зоне) традиционные металлические абатменты (например, из сплавов золота) могут вызывать сероватый оттенок на десне, нарушая эстетику. Хотя титановые абатменты могут представлять аналогичный риск, их серый оттенок обычно светлее, и его можно полностью избежать, выбрав цельнокерамические абатменты или титановые абатменты с керамическим или циркониевым покрытием. В качестве материала для абатментов или каркасов титан также обеспечивает надежную опору для цельнокерамических реставраций, позволяя добиться естественных эстетических результатов.

4. Общие области применения титана в стоматологии
Титан широко используется в различных областях реставрации зубов, имплантации, ортодонтии и хирургии:
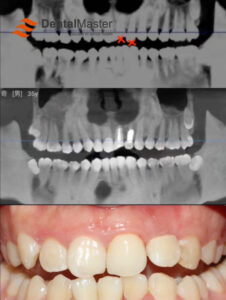
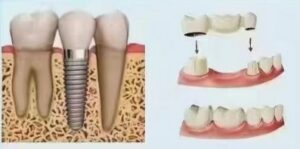
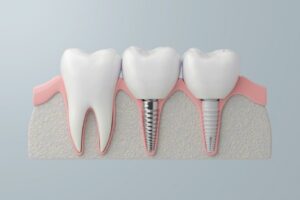
4.1 Зубные имплантаты:
Это самое центральное и успешное применение титана в стоматологии. Титановые имплантаты служат в качестве искусственных зубных корней, хирургически вживляемых в челюстную кость для поддержки надстроек (коронок, мостов, зубных протезов). Их конструкции (корневидные, цилиндрические, клинковые), обработка поверхности (SLA, SLActive, анодирование и т.д.) и методы соединения (внутренний шестигранник, конус Морзе, переключение платформы) продолжают развиваться, чтобы соответствовать различным состояниям кости, потребностям протезирования и эстетическим требованиям. Показатель долгосрочного успеха (более 10 лет) часто превышает 95% при строгих показаниях.
4.2 Абатменты и компоненты протезов:
Абатменты: Ключевые компоненты, соединяющие платформу имплантата с супраструктурой. Они могут быть изготовлены из титана (CP Ti или сплава), диоксида циркония или их комбинации (титановая основа + циркониевая вершина). Титановые абатменты Прочные, надежные в соединении с имплантатами и биосовместимые, они являются основным выбором, особенно подходящим для задних областей или угловых абатментов.
Протезные винты: Используются для крепления абатментов или реставраций к имплантатам, обычно изготавливаются из высокопрочных титановых сплавов (например, Ti-6Al-4V). Они требуют чрезвычайно высокой усталостной прочности и точности размеров.
Рукава, разъемы: В сложных ортопедических конструкциях (например, балочных зубных протезах) титановые соединители обеспечивают стабильность и прочность.
4.3 Ортодонтические дуги и брекеты:
Арки: Бета-титановые сплавы (например, ТМА - титано-молибденовый сплав) предпочтительны в несъемной ортодонтии благодаря более низкому модулю упругости (более мягкие, постоянные усилия), высокому пределу упругости (большой диапазон деформации), хорошей формуемости и биосовместимости. Обычно используются на поздних этапах для тонкой регулировки.
Кронштейны: Металлические брекеты из титана используются в основном для пациентов с аллергией на никель, обладая хорошей биосовместимостью и достаточной прочностью.
4.4 Хирургические инструменты и приборы:
Отличная прочность, малый вес и устойчивость к коррозии делают титан идеальным материалом для производства высокоточных и долговечных изделий. стоматологические хирургические инструментыТакие, как хирургические направляющие для имплантатов, остеотомы, иглодержатели, ретракторы и носители/ключи для имплантатов. Его немагнитная природа также подходит для специальных условий обследования (например, МРТ).
4.5 Коронки, мосты и каркасы (каркасы зубных протезов):
Crown/Bridge Frameworks: Коммерчески чистый титан (в основном 1 и 2 класса) может быть отлит или отфрезерован в CAD/CAM для изготовления коронок или мостовидных протезов. К преимуществам относятся легкость, хорошая биосовместимость и рентгенопрозрачность. К недостаткам относятся трудности литья (окисление, усадка) и эстетика, уступающая цельнокерамической (требуется облицовка фарфором, а соединение с титаном является ключевой проблемой).
Каркасы съемных зубных протезов: По сравнению с традиционными кобальто-хромовыми сплавами, титановые каркасы значительно снижают вес, повышают комфорт ношения, улучшают биосовместимость, меньше влияют на вкус и не вызывают аллергии. Обычно используется в базисах и кламмерах частичных съемных протезов.

5. Обработка титана и обработка поверхности: Ключ к формированию характеристик
Характеристики титана зависят не только от присущих ему свойств, но и от методов обработки и состояния поверхности, что особенно важно для остеоинтеграции имплантата.
5.1 Методы обработки:
Холодная обработка: Такие методы, как прокатка и волочение, используются для производства титановой проволоки (ортодонтические дуги), листов (каркасы) и стержней (обработанные абатменты), заготовки для имплантатов). Повышает прочность, но снижает пластичность.
Обработка (субтрактивное производство): Основной метод изготовления имплантатов, абатментов и индивидуальных компонентов протезов. Требуются высокожесткие станки, специализированные инструменты (твердосплавные, с алмазным напылением) и охлаждающая жидкость (строго предотвращающая окисление). Необходима чрезвычайно высокая точность (микронный уровень), при этом стоимость обработки относительно высока. Технология CAD/CAM широко применяется в этой области для высокоточного и эффективного изготовления на заказ.
Кастинг: Используется для изготовления каркасов коронок/мостов и конструкций зубных протезов. Должно производиться в вакууме или в среде инертного газа (аргона) для предотвращения окисления и поглощения газов (водорода, кислорода). Отливки часто имеют усадку, внутренние дефекты и поверхностные реакционные слои (α-case), требующие последующей обработки (пескоструйная обработка, кислотное травление, горячее изостатическое прессование - HIP) для улучшения характеристик.
Аддитивное производство (3D-печать): Такие технологии, как выборочное лазерное плавление (SLM) и электронно-лучевое плавление (EBM), позволяют изготавливать сложные титановые детали (индивидуальные абатменты, каркасы, хирургические направляющие, пористые имплантаты) непосредственно по цифровым 3D-моделям. Эти методы обеспечивают высокую свободу дизайна, эффективное использование материалов и возможность создания сложных внутренних структур (например, биомиметических пористых структур для врастания кости). Это одно из основных направлений будущего развития (подробнее см. раздел 7).
5.2 Технологии модификации поверхности:
Микро- и наноразмерная морфология, химический состав и смачиваемость (гидрофильность) поверхности имплантата оказывают решающее влияние на адсорбцию белков, поведение клеток (адгезию, пролиферацию, дифференцировку), а также на скорость и качество остеоинтеграции. Основные технологии включают:
Механическая обработка:
- Обработка/шлифовка: Образует гладкие или регулярно текстурированные поверхности. Часто использовался на ранних этапах применения, в настоящее время в основном применяется в области шейки имплантата (для уменьшения прикрепления налета).
- Пескоструйная обработка: Поверхности подвергаются бомбардировке глиноземом (Al₂O₃), диоксидом титана (TiO₂) или биосовместимыми керамическими частицами (например, гидроксиапатитом, HA) для создания макроскопической шероховатости (микронный масштаб), увеличения площади поверхности и способности к механическому сцеплению. Часто сочетается с кислотным травлением.
Химическая обработка:
- Кислотная гравюра: Использует сильные кислоты (например, смешанные HCl/H₂SO₄, HF/HNO₃) для растворения поверхности титана, формируя сложную пористую морфологию микронного или даже наноразмера. Увеличивает удельную площадь поверхности и улучшает смачиваемость. Является основой многих композитных методов обработки.
- Щелочная термическая обработка: Титан погружается в раствор NaOH, затем нагревается, образуя на поверхности слой геля титаната натрия, который в жидкостях организма может превращаться в костеподобный апатит, значительно повышая биоактивность.
Физико-химическая обработка:
- Пескоструйная обработка, крупнозернистая обработка, кислотное травление (SLA®): Сначала пескоструйная обработка создает шероховатость микронного масштаба, а затем кислотное травление удаляет остатки обработки и добавляет наноразмерные структуры. В настоящее время это одна из наиболее коммерчески успешных, широко используемых и клинически поддерживаемых технологий обработки поверхности, значительно ускоряющая остеоинтеграцию и улучшающая первоначальную стабильность.
- Гидрофильная SLA (SLActive®): После обработки SLA поверхности хранятся/упаковываются под защитой азота или в солевом растворе для сохранения высокой поверхностной энергии и гидрофильности (контактный угол около 0°). Гидрофильность способствует быстрому распространению крови и жидкостей на поверхности имплантата, ускоряет формирование фибринового матрикса и привлечение остеобластов, что позволяет добиться более быстрого заживления кости (недели вместо месяцев по сравнению с традиционным SLA).
- Анодное окисление: Подача напряжения в электролит позволяет контролировать рост толстой, пористой пленки TiO₂ (которая может включать элементы кальция и фосфата) на поверхности титана. Толщина пленки (которая влияет на интерференцию цветов при изготовлении эстетических абатментов), пористость и состав могут точно контролироваться, улучшая коррозионную стойкость, биоактивность и (при определенных условиях) антибактериальные свойства.
Технологии нанесения покрытий:
- Гидроксиапатитовое (HA) покрытие: Нанесение биоактивного керамического слоя HA на титановые поверхности с помощью таких методов, как плазменное напыление (TPS). Предназначен для создания прямого остеокондуктивного/остеоиндуктивного интерфейса. Однако существуют проблемы, связанные с адгезией и долгосрочной стабильностью покрытия (возможны деградация и отслоение), и этот метод используется менее широко, чем SLA.
- Другие покрытия с биоактивными молекулами: Такие как костные морфогенетические белки (BMP), пептиды (RGD), факторы роста и т.д., которые в настоящее время находятся на стадии исследований, направленных на обеспечение более активных биологических сигналов на поверхности.
5.3 Влияние обработки поверхности на биологические реакции и клинические показатели:
- Ускоренная остеоинтеграция: Шероховатые (SLA, SLActive) и биоактивированные (HA-покрытие, щелочная термообработка) поверхности значительно сокращают период заживления имплантата (с 3-6 месяцев на традиционных гладких поверхностях до 3-6 недель или даже меньше), позволяя сразу же или раньше нагружать его и повышая удовлетворенность пациента.
- Улучшенная биомеханическая фиксация: Микро/наноразмерные шероховатые поверхности увеличивают площадь контакта кости с имплантатом (BIC%) и формируют механические взаимосвязанные структуры, значительно улучшая начальную стабильность имплантата и долгосрочную несущую способность.
- Влияние на прикрепление мягких тканей: Характеристики поверхности (такие как гладкость и гидрофильность) трансгингивальной части (шейки) имплантата имеют решающее значение для прикрепления эпителиальных клеток и фибробластов, формируя хорошее уплотнение мягких тканей (биологическая ширина), что является ключом к предотвращению бактериальной инвазии и поддержанию здоровья периимплантита.
- Потенциальные риски: Чрезмерно шероховатые или микротрещиноватые поверхности могут увеличить риск колонизации бактерий, что требует более высоких стандартов контроля периимплантита. Долгосрочная стабильность покрытий (таких как HA) все еще нуждается в дополнительных доказательствах.

6. Проблемы и ограничения
Несмотря на то, что титан достиг больших успехов в стоматологии, некоторые проблемы остаются:
6.1 Затраты на сырье и переработку:
- Добыча и обогащение титановых руд (рутила, ильменита) по технологиям Кролла или Хантера являются энергоемкими и сложными, в результате чего стоимость сырья значительно выше, чем у нержавеющей стали или кобальто-хромовых сплавов.
- Обработка титана (литье, механическая обработка, 3D-печать) сложна, требует специализированного оборудования, строгого контроля окружающей среды (защита инертным газом) и высококвалифицированных работников, что еще больше увеличивает стоимость производства. Это делает конечные стоматологические изделия на основе титана (особенно имплантаты и индивидуальные реставрации) относительно дорогими.
6.2 Аллергия или редкая чувствительность:
- Обычно считается, что титан обладает крайне низкой аллергенностью. Однако редкие, но документально подтвержденные клинические случаи свидетельствуют о гиперчувствительности замедленного типа (аллергическая реакция IV типа) у очень небольшого числа людей на металл титана или элементы сплава (например, алюминий, ванадий, примеси никеля).
- Симптомы могут включать постоянное воспаление околоимплантатной области, покраснение и отек слизистой оболочки, боль и даже нарушение остеоинтеграции.
- Диагностика затруднена из-за отсутствия высокоспецифичных и чувствительных стандартизированных тестов на аллергию к титану (например, интерпретация патч-теста вызывает споры).
- Несмотря на низкую частоту встречаемости (гораздо ниже, чем при аллергии на никель), ведение пациентов с подозрением (например, переход на имплантаты из диоксида циркония) и изучение механизма остаются важными клиническими темами.
6.3 Износ и электрохимическая коррозия в смешанных металлических средах:
- Фреттинг/коррозия: Системы имплантатов включают множество металлических интерфейсов (например, винты абатмента и внутренняя резьба имплантата, соединения абатмент-имплантат). Функциональные микродвижения (жевательные нагрузки, окклюзия) вызывают фреттинг-износ, который повреждает защитные оксидные пленки и обнажает свежий металл.
- Гальваническая коррозия: Когда в полости рта находятся различные металлы (например, титановые имплантаты + золотые коронки, ортодонтическая проволока из нержавеющей стали + титановые брекеты), соединенные слюной (электролитом), разность потенциалов вызывает ускоренное коррозионное растворение металла с более низким потенциалом (анода, например, титана).
- Даже различные марки или состояния поверхности титана могут иметь незначительные потенциальные различия.
- Щелевая коррозия: В плотно прилегающих, но не абсолютно герметичных металлических соединениях (например, на стыке абатмента и имплантата) снижение концентрации кислорода, понижение pH и накопление хлорид-ионов в щелях могут вызывать локальную коррозию.
- Последствия: Эти коррозионные процессы могут ослабить механическую прочность, привести к попаданию ионов/частиц металла в окружающие ткани, что может вызвать местные или системные реакции (например, аллергию, воспаление), а также повлиять на долгосрочную стабильность и срок службы имплантатов. Строгий контроль совместимости материалов, оптимизация конструкций соединений (например, уплотнения с конусом Морзе) и повышение точности изготовления для уменьшения микроподвижности являются ключевыми мерами противодействия.
7.Будущее развитие и инновации
Для преодоления существующих проблем и дальнейшего улучшения характеристик исследования стоматологических материалов на основе титана сосредоточены на следующих направлениях:
7.1 Разработка новых сплавов на основе титана:
- Оптимизация сплавов, не содержащих алюминия и ванадия: Продолжайте продвигать и оптимизировать альтернативные сплавы, такие как Ti-6Al-7Nb, и углубленно разрабатывайте титановые сплавы β-типа с превосходными характеристиками и лучшей биосовместимостью (например, сплавы системы Ti-Nb-Zr-Ta). Цель - добиться сверхнизкого модуля упругости, близкого к модулю упругости костной ткани, более высоких пределов усталости и превосходной коррозионной стойкости.
- Титан-циркониевые сплавы (Ti-Zr): Сплавы, представленные Roxolid® (Ti-15Zr), были успешно коммерциализированы. Их прочность (>850 МПа) значительно выше, чем у коммерчески чистого титана (~550 МПа) и близка к Ti-6Al-4V (~900 МПа), при этом биосовместимость сопоставима с чистым титаном, а способность к остеоинтеграции превосходна. Будущие направления включают оптимизацию содержания Zr, изучение сплавов Ti-Zr в сочетании с другими элементами (такими как Nb, Ta) и расширение их применения на более широкий спектр компонентов для восстановления имплантатов (например, абатментные винты, персонализированные абатменты).
- Низкомодульные высокопрочные сплавы: Разработка сплавов с наноструктурами или особыми фазовыми составами, позволяющих преодолеть традиционные ограничения по соотношению прочности и модуля упругости обычных сплавов.
7.2 Глубокая интеграция аддитивного производства (3D-печати) и цифровой стоматологии:
- Индивидуальные сложные конструкции: Технологии SLM/EBM позволяют точно изготавливать сложные геометрические формы, невозможные при использовании традиционных процессов, например, высокобиомиметичные персонализированные имплантаты с внутренней пористой градиентной структурой (способствующие врастанию кости и васкуляризации), анатомически подобранные персонализированные абатменты и скаффолды для наращивания кости (Мембраны GBR, титановые сетки).
- Оптимизация топологии: С помощью компьютерных алгоритмов проектирование конструкций имплантатов или реставрационных каркасов с оптимальным распределением материала, минимальным весом и наиболее равномерным распределением нагрузки на основе анализа силы.
- Интегрированный рабочий процесс: 3D-печать легко интегрируется в процессы цифровой стоматологии (сканирование полости рта/получение данных компьютерной томографии → проектирование CAD → печать CAM), обеспечивая полностью отслеживаемое, эффективное и точное производство реставраций/направляющих имплантатов/имплантатов. Снижение затрат и повышение доступности являются ключевыми факторами для более широкого внедрения.
7.3 Применение нанотехнологий для создания поверхности титана:
Создание наноструктур: С помощью химических (например, двойное кислотное травление, щелочно-термическая обработка), физических (например, лазерная абляция, ионный пучок) или электрохимических (например, анодирование) методов на поверхности титана точно создаются нанотрубки, нанопоры, наночастицы, наноморщины и другие наноструктуры. Эти наноразмерные элементы более эффективно имитируют внеклеточный матрикс (ECM), напрямую регулируя поведение клеток (остеобластов, стволовых клеток), включая адгезию, распространение, миграцию, пролиферацию и дифференцировку, и даже влияя на экспрессию генов.
Функционализированные нанопокрытия:
Антибактериальные покрытия: Загрузка антибактериальных агентов, таких как наночастицы серебра (AgNPs), наночастицы оксида цинка (ZnO NPs), антимикробные пептиды (AMPs), хитозан и т.д., для придания длительных антибактериальных свойств поверхности и активной профилактики периимплантита.
Остеогенные/ангиогенные промотирующие покрытия: Загрузка факторов роста (например, BMP-2, VEGF), биоактивных ионов (например, Sr²⁺, Mg²⁺, Li⁺) или небольших молекулярных препаратов для точной регуляции локальной микросреды, способствующей быстрой и качественной регенерации кости и васкуляризации.
Умные реагирующие покрытия: Разработка "умных" покрытий, реагирующих на изменения в среде полости рта (например, на снижение pH или активацию бактериальных ферментов) и высвобождающих антибактериальные или противовоспалительные препараты для лечения по требованию.
Улучшение долговременной стабильности поверхности: Изучение стабильности, поведения при деградации и биологической реакции наноструктур во время длительной эксплуатации.
Заключение
Титан и титановые сплавы заняли ключевое положение в современной стоматологии, особенно в дентальной имплантологии, благодаря своей непревзойденной биосовместимости, отличным механическим свойствам (особенно высокому соотношению прочности и веса), исключительной коррозионной стойкости и уникальной способности способствовать остеоинтеграции. От имплантатов, служащих искусственными корнями зубов, до абатментов для соединения и перехода, опорных лесов и эффективных ортодонтических инструментов - титановые материалы используются во всех аспектах реставрации зубов, значительно улучшая восстановление функций полости рта и эстетическое восстановление.
Несмотря на такие проблемы, как стоимость, редкие аллергические реакции и коррозия в смешанных металлических средах, достижения в области материаловедения и технологии производства продолжают открывать новые пути. Новые сплавы на основе титана (такие как высокопрочные сплавы Ti-Zr и низкомодульные сплавы β-типа) направлены на улучшение характеристик при обеспечении биобезопасности; аддитивное производство (3D-печать) открыло новую эру высоко персонализированных реставраций со сложной структурой и производства имплантатов; а наноструктурная инженерия поверхности позволяет с беспрецедентной точностью контролировать интерфейс материал-биология, наделяя титановые поверхности антибактериальными, остеогенными и даже интеллектуальными отзывчивыми функциями.
В будущем материалы на основе титана останутся "золотым стандартом" и ключевым носителем инноваций в восстановлении зубов с помощью имплантатов. Благодаря постоянным инновациям в области материалов, передовым производственным процессам и точному дизайну поверхности, применение титана в стоматологии станет более минимально инвазивным, быстрым, долговечным, персонализированным и безопасным, что в конечном итоге обеспечит пациентов решениями для восстановления полости рта, превосходящими как по функциональности, так и по эстетике, с улучшенным долгосрочным прогнозом, значительно повышающими качество жизни пациентов. Легендарная история титана в стоматологии еще далека от завершения и продолжает писать новые блестящие главы.
Ссылки
Бронемарк, П. И., Аделл, Р., Брейн, У., Ханссон, Б. О., Линдстрем, Й., и Олссон, А. (1977). Внутрикостное крепление зубных протезов. I. Экспериментальные исследования. Скандинавский журнал пластической и реконструктивной хирургии, 11(3), 81-100.
(Ввел концепцию остеоинтеграции и создал биологическую основу для титановых имплантатов).
ASTM International. (2019). ASTM F67-13: Стандартная спецификация на нелегированный титан для хирургических имплантатов. ASTM.
ASTM International. (2020). ASTM F136-13: Стандартная спецификация на деформируемый сплав титан-6алюминий-4ванадий ELI для применения в хирургических имплантатах. ASTM.
(Определяет стандарты медицинского класса для коммерчески чистого титана и сплава Ti-6Al-4V).
Buser, D., Broggini, N., Wieland, M., et al. (2004). Улучшенное прилегание кости к химически модифицированной титановой поверхности SLA. Журнал стоматологических исследований, 83(7), 529-533.
(Классическое исследование, демонстрирующее ускоренную остеоинтеграцию с помощью модификации поверхности SLA).
Chiapasco, M., Casentini, P., & Zaniboni, M. (2012). Процедуры наращивания костной ткани в стоматологии на имплантатах. Международный журнал челюстно-лицевых имплантатов, 27(Suppl), s183-s203.
(Клинические данные по использованию сплава Ti-15Zr (Roxolid®) в имплантатах узкого диаметра).
Курода, Д., Нииноми, М., Моринага, М. и др. (1998). Дизайн и механические свойства новых титановых сплавов типа β для материалов имплантатов. Материаловедение и инженерия: A, 243(1-2), 244-249.
(Демонстрирует биомеханические преимущества титановых сплавов с низким модулем упругости β-типа).
Ван Ноорт, Р. (2012). Будущее стоматологических устройств - за цифровыми технологиями. Стоматологические материалы, 28(1), 3-12.
(Рассматриваются перспективы применения цифровых производственных технологий, таких как 3D-печать, для изготовления зубных имплантатов).
Мендонса, Г., Мендонса, Д. Б., Арагао, Ф. Ж., и Купер, Л. Ф. (2008). Продвижение технологии поверхности зубных имплантатов - от микронов до нанотопографии. Биоматериалы, 29(28), 3822-3835.
(Обсуждается, как наноразмерные топографии поверхности модулируют клеточное поведение).
Сиддики, А., Пейн, А. Г., Де Сильва, Р. К., и Дункан, В. Дж. (2011). Аллергия на титан: Обзор литературы. Международный журнал челюстно-лицевых имплантатов, 26(4), 743-750.
(Систематический обзор по эпидемиологии аллергии на титан и проблемам диагностики).
Reclaru, L., & Meyer, J. M. (1994). Электрохимическая коррозия в реставрационной стоматологии. Стоматологические клиники Северной Америки, 38(2), 319-332.
(Изучение механизмов электрохимической коррозии в полости рта с использованием нескольких металлов).
Пьетурссон, Б. Э., Тома, Д., Юнг, Р. и др. (2012). Систематический обзор выживаемости и частоты осложнений несъемных зубных протезов с опорой на имплантаты (FDP) после среднего периода наблюдения не менее 5 лет. Клинические исследования имплантатов полости рта, 23(Suppl 6), 22-38.
(Приводятся научно обоснованные данные о выживаемости имплантатов в течение 10 лет).