Il titanio e le sue leghe sono diventati i materiali cardine della moderna protesi dentaria grazie alla loro eccellente biocompatibilità, alle proprietà meccaniche e alla capacità di osteointegrazione. Questo articolo descrive sistematicamente la classificazione dei materiali in titanio, le loro proprietà principali, la loro ampia applicazione in campo odontoiatrico (con gli impianti come focus), le tecnologie di lavorazione e il loro impatto, le sfide attuali e le prospettive, come le nuove leghe, la produzione additiva e la nanoingegneria di superficie, con l'obiettivo di fornire riferimenti teorici per la pratica clinica e la ricerca.

1. Introduzione
Il titanio (Ti), 22° elemento della tavola periodica, è un metallo di transizione bianco-argento. Dagli anni '50, quando lo studioso svedese Per-Ingvar Brånemark scoprì che il titanio poteva formare una connessione diretta, funzionale e strutturale con il tessuto osseo (nota come "osteointegrazione"), il titanio ha aperto un brillante capitolo nel campo biomedico, soprattutto nell'implantologia dentale. La sua combinazione unica di proprietà soddisfa perfettamente i rigorosi requisiti dei materiali per la riabilitazione orale: eccellente biocompatibilità per evitare il rigetto, resistenza specifica estremamente elevata per sopportare le forze masticatorie, eccezionale resistenza alla corrosione contro l'erosione della saliva e buona osteoconduttività per garantire la stabilità a lungo termine. Il successo e la prevedibilità dei trattamenti implantari dipendono fortemente da queste caratteristiche fondamentali del titanio, che lo rendono l'insostituibile "re dei biomateriali" nei restauri dentali, in particolare per la riabilitazione della perdita dei denti.
2. Classificazione del titanio e delle leghe di titanio
I materiali in titanio utilizzati in campo dentale possono essere classificati in due categorie principali in base alla loro composizione e alle loro proprietà:
- 2.1 Titanio commercialmente puro (CP Ti):
- Secondo gli standard ASTM (ad esempio, F67), il CP Ti è suddiviso in gradi da 1 a 4 in base al contenuto di elementi interstiziali come ossigeno e ferro.
- Caratteristiche: Offre la migliore biocompatibilità (è il più inerte), un'eccellente resistenza alla corrosione e una buona plasticità, che lo rende facile da lavorare. Tuttavia, la sua resistenza (soprattutto allo snervamento e alla fatica) è relativamente bassa.
- Applicazioni dentali: Utilizzato principalmente per impianti, abutment, strutture di corone e ponti e brackets ortodontici in cui le esigenze di resistenza non sono estreme. Il CP Ti Grado 4 è il più utilizzato.
- 2.2 Leghe di titanio:
- Aggiungendo elementi di lega (ad esempio, Al, V, Nb, Zr, Mo, Ta), si migliorano le proprietà meccaniche del titanio.
- Lega rappresentativa - Ti-6Al-4V (grado 5):
- La classica lega di titanio a fase α+β (l'alluminio 6% stabilizza la fase α, il vanadio 4% stabilizza la fase β).
- Caratteristiche: Molto più forte del CP Ti (circa il doppio della resistenza del CP Ti grado 4), eccellenti proprietà di fatica e buona resistenza alla corrosione. Tuttavia, esistono preoccupazioni sulla potenziale tossicità biologica del vanadio (V) e dell'alluminio (Al) (nonostante le limitate evidenze cliniche) e il suo modulo elastico è ancora superiore a quello dell'osso.
- Altre leghe nuove/specifiche per l'odontoiatria:
- Ti-6Al-7Nb, Ti-5Al-2,5Fe: Progettato per sostituire il Ti-6Al-4V, evitando il vanadio per una migliore biocompatibilità.
- Leghe di titanio di tipo β (ad esempio, Ti-13Nb-13Zr, Ti-12Mo-6Zr-2Fe - TMZF, Ti-35Nb-7Zr-5Ta): Utilizzano niobio (Nb), tantalio (Ta), zirconio (Zr) e molibdeno (Mo) come principali elementi di lega.
- Caratteristiche: Modulo elastico più basso (più vicino all'osso, riducendo la schermatura delle sollecitazioni), maggiore resistenza alla fatica e alla frattura, eccellente resistenza alla corrosione, assenza di elementi controversi (come V e Al) e biocompatibilità superiore. Questi aspetti sono attualmente un punto caldo della ricerca.
- Leghe Ti-Zr (ad esempio, Roxolid® - Ti-15Zr): Sviluppato specificamente per l'odontoiatria, offre una resistenza superiore a quella del CP Ti e si avvicina a quella del Ti-6Al-4V, ma con una biocompatibilità più vicina a quella del titanio puro e un modulo elastico moderato. Particolarmente adatto per impianti di piccolo diametro.
Tabella 1: Confronto delle proprietà del titanio dentale comune e delle leghe di titanio
| Tipo di materiale | Grado tipico | Composizione principale | Vantaggi | Limitazioni | Principali applicazioni dentali |
|---|---|---|---|---|---|
| Ti commercialmente puro | Grado 1 | >99% Ti | Migliore biocompatibilità, eccellente resistenza alla corrosione, duttile | Forza più bassa | Parti a parete sottile, membrane |
| Grado 2 | >98,9% Ti | Buone prestazioni complessive (equilibrio tra biocompatibilità, resistenza alla corrosione, forza, plasticità) | Forza moderata | Abutment, piccoli restauri, brackets | |
| Grado 3 | >98,8% Ti | Resistenza superiore al grado 2 | Leggermente meno duttile del grado 2 | Impianti (alcuni), monconi, strutture | |
| Grado 4 | >98,6% Ti | CP Ti più forte | Duttilità inferiore rispetto al CP Ti di grado inferiore | Impianti mainstream, abutment, fili d'arco | |
| α+β Leghe di titanio | Ti-6Al-4V (Gr5) | Ti-6Al-4V | Alta resistenza, eccellente resistenza alla fatica | Contiene Al/V (potenziale biotossicità), elevato modulo elastico | Impianti in aree ad alto carico, connettori, strumenti chirurgici |
| Ti-6Al-7Nb | Ti-6Al-7Nb | Resistenza vicina al Gr5, assenza di V (migliore biocompatibilità) | Contiene Al | Impianti (sostituto Gr5) | |
| Leghe di tipo β | Ti-13Nb-13Zr | Ti-13Nb-13Zr | Basso modulo elastico, eccellente biocompatibilità, assenza di Al/V | Elaborazione complessa | Impianti (per attenuare la schermatura delle sollecitazioni), fili ortodontici |
| Ti-12Mo-6Zr-2Fe (TMZF) | Ti-12Mo-6Zr-2Fe | Basso modulo elastico, elevata resistenza, buona resistenza alla corrosione | Contiene Fe (dati biologici a lungo termine limitati) | Impianti, impianti ortopedici | |
| Lega specifica per il settore dentale | Ti-15Zr (Roxolid®) | Ti-15Zr | Molto più resistente del CP4, vicino al Gr5, biocompatibilità vicina al CP Ti | Costo più elevato | Impianti di piccolo diametro/di cresta stretta |
(Nota: questa tabella è un confronto semplificato. I parametri esatti delle prestazioni devono fare riferimento agli standard dei materiali e ai dati del produttore. Modulo elastico: CP Ti ~100-110 GPa, Ti-6Al-4V ~110-115 GPa, leghe β ~55-85 GPa, osso corticale ~10-30 GPa)
3. I principali vantaggi del titanio in odontoiatria
Il titanio e le sue leghe presentano vantaggi ineguagliabili nelle applicazioni dentali:
- 3.1 Eccezionale biocompatibilità e resistenza alla corrosione:
- Biocompatibilità: Il titanio può formare spontaneamente un film passivo di biossido di titanio (TiO₂) denso, stabile e inerte in ambienti fisiologici. Questa pellicola isola efficacemente il rilascio di ioni metallici nei tessuti circostanti, riducendo al minimo l'infiammazione e il rigetto immunitario - un prerequisito per l'osteointegrazione. Numerosi studi clinici e dati di follow-up a lungo termine confermano l'eccellente risposta dei tessuti agli impianti in titanio.
- Resistenza alla corrosione: Lo strato passivo di TiO₂ ha una forte resistenza ai fluidi corporei (saliva, sangue, fluido interstiziale), ai fluoruri (da dentifrici e collutori) e alle fluttuazioni del pH orale (ad esempio, da cibi e bevande acidi). Anche durante il servizio a lungo termine, problemi come vaiolatura, corrosione interstiziale o cricca da corrosione da stress sono estremamente rari, garantendo la stabilità chimica a lungo termine e la sicurezza degli impianti nel difficile ambiente orale.
- 3.2 Elevato rapporto resistenza/peso (elevata resistenza specifica):
Il titanio ha una densità significativamente inferiore (~4,5 g/cm³) rispetto all'acciaio inossidabile (~8 g/cm³) e alle leghe di cobalto-cromo (~8,5 g/cm³), ma la sua resistenza (soprattutto quella delle leghe di titanio) è paragonabile o addirittura superiore a questi materiali. Ciò significa che i restauri o gli impianti in titanio possono fornire una capacità di carico sufficiente (sopportare forze masticatorie, di solito fino a diverse centinaia di newton) pur essendo più leggeri, riducendo così il carico sui tessuti di supporto e migliorando il comfort del paziente. - 3.3 Eccellente capacità di osteointegrazione:
Questo è il vantaggio principale del titanio come materiale implantare. Lo strato di TiO₂ sulla superficie del titanio è bioattivo e può adsorbire selettivamente le proteine del sangue e dei fluidi corporei (come il fibrinogeno e la fibronectina), promuovendo l'adesione, la proliferazione e la differenziazione degli osteoblasti. Alla fine, il nuovo tessuto osseo può depositarsi direttamente e legarsi saldamente alla superficie del titanio, formando una connessione strutturale e funzionale diretta senza un'interfaccia di tessuto connettivo fibroso. Questa integrazione diretta osso-impianto fornisce la base biologica per la ritenzione stabile a lungo termine dell'impianto. - 3.4 Radiolucenza e vantaggi estetici:
Radiolucenza: Il titanio ha un'attenuazione dei raggi X molto più bassa rispetto ai metalli tradizionali come le leghe d'oro e le leghe di cobalto-cromo. Nelle radiografie (pellicole periapicali, pellicole panoramiche, CBCT), gli impianti in titanio appaiono come immagini a densità relativamente bassa, consentendo una chiara visualizzazione della struttura ossea circostante. Ciò facilita la valutazione accurata da parte dei medici dello stato di osteointegrazione, delle variazioni del livello osseo marginale e della salute perimplantare, rendendola fondamentale per il monitoraggio a lungo termine.
Vantaggio estetico: Nel caso di gengive sottili o di impianti posizionati superficialmente (soprattutto nella zona anteriore), gli abutment metallici tradizionali (ad esempio, leghe d'oro) possono causare una colorazione grigiastra attraverso la gengiva, compromettendo l'estetica. Sebbene gli abutment in titanio possano comportare un rischio simile, la loro tonalità grigia è generalmente più chiara e può essere completamente evitata scegliendo abutment interamente in ceramica o abutment in titanio con rivestimenti in ceramica o zirconia. Come materiale per gli abutment o le strutture, il titanio fornisce anche un supporto affidabile per i restauri in ceramica integrale, consentendo risultati estetici dall'aspetto naturale.

4. Applicazioni comuni del titanio in odontoiatria
Il titanio è ampiamente utilizzato in vari settori del restauro dentale, dell'implantologia, dell'ortodonzia e della chirurgia:
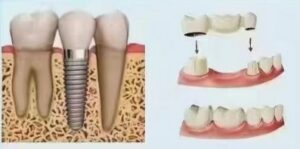
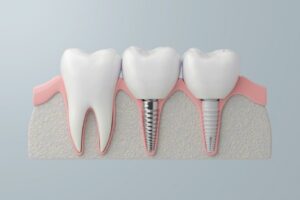
4.1 Impianti dentali:
Si tratta dell'applicazione più centrale e di successo del titanio in odontoiatria. Impianti in titanio servono come radici dentali artificiali, inserite chirurgicamente nell'osso mascellare per sostenere sovrastrutture (corone, ponti, overdenture). I loro design (a forma di radice, cilindrico, a lama), i trattamenti superficiali (SLA, SLActive, anodizzazione, ecc.) e i metodi di connessione (esagono interno, cono Morse, commutazione di piattaforma) continuano a evolversi per soddisfare le varie condizioni ossee, le esigenze protesiche e le richieste estetiche. Il tasso di successo a lungo termine (oltre 10 anni) supera spesso il 95% in presenza di indicazioni rigorose.
4.2 Monconi e componenti protesici:
Monconi: I componenti chiave che collegano la piattaforma implantare alla sovrastruttura. Possono essere realizzati in titanio (CP Ti o lega), zirconia o una combinazione (base in titanio + top in zirconia). Abutment in titanio sono robusti, affidabili in connessione con gli impianti e biocompatibili, il che li rende una scelta mainstream, particolarmente adatta alle regioni posteriori o agli abutment angolati.
Viti protesiche: Utilizzati per fissare abutment o restauri agli impianti, solitamente realizzati in leghe di titanio ad alta resistenza (ad esempio, Ti-6Al-4V). Richiedono una resistenza alla fatica e una precisione dimensionale estremamente elevate.
Manicotti, Connettori: Nelle strutture protesiche complesse (come le overdenture con barra), i connettori in titanio garantiscono stabilità e resistenza.
4.3 Fili e brackets ortodontici:
Fili ad arco: Le leghe di beta titanio (ad es. TMA - lega di titanio-molibdeno) sono favorite nell'ortodonzia fissa grazie al loro modulo elastico più basso (forze più morbide e continue), all'elevato limite elastico (ampio intervallo di deformazione), alla buona formabilità e alla biocompatibilità. Si usano comunemente nelle fasi successive per le regolazioni fini.
Staffe: I brackets in metallo di titanio sono utilizzati principalmente per i pazienti allergici al nichel, offrendo una buona biocompatibilità e una resistenza sufficiente.
4.4 Strumenti e attrezzi chirurgici:
L'eccellente forza, la leggerezza e la resistenza alla corrosione del titanio lo rendono ideale per la produzione di prodotti di alta precisione e di lunga durata. strumenti chirurgici dentalicome le guide chirurgiche per impianti, gli osteotomi, i portaaghi, i divaricatori e i porta-impianti. La sua natura amagnetica si adatta anche ad ambienti di esame speciali (ad esempio, la risonanza magnetica).
4.5 Corone, ponti e strutture (strutture per protesi):
Cornici Crown/Bridge: Il titanio commercialmente puro (principalmente gradi 1 e 2) può essere fuso o fresato con CAD/CAM per fabbricare corone o ponti. I vantaggi sono la leggerezza, la buona biocompatibilità e la radiotrasparenza. Gli svantaggi includono difficoltà di fusione (ossidazione, contrazione) ed estetica inferiore alla ceramica integrale (è necessario rivestire la porcellana e l'adesione al titanio è una sfida fondamentale).
Strutture per protesi rimovibili: Rispetto alle tradizionali leghe di cobalto-cromo, le strutture in titanio riducono significativamente il peso, migliorano il comfort di calzata, aumentano la biocompatibilità, hanno un minore impatto sul gusto e non presentano problemi di allergie. Sono comunemente utilizzate nelle basi e nelle chiusure delle protesi parziali rimovibili.

5. Lavorazione e trattamento superficiale del titanio: La chiave per modellare le prestazioni
Le prestazioni del titanio dipendono non solo dalle sue proprietà intrinseche, ma anche dai metodi di lavorazione e dalle condizioni della superficie, particolarmente importanti per l'osteointegrazione degli impianti.
5.1 Tecniche di elaborazione:
Lavorazione a freddo: Come la laminazione e la trafilatura, utilizzate per produrre fili di titanio (archi ortodontici), lastre (strutture) e barre (abutment lavorati), grezzi per impianti). Aumenta la resistenza ma riduce la duttilità.
Lavorazione (produzione sottrattiva): È il metodo principale per la produzione di impianti, abutment e componenti protesici personalizzati. Richiede macchine ad alta rigidità, utensili specializzati (in carburo, rivestiti di diamante) e refrigerante (che impedisce rigorosamente l'ossidazione). È necessaria una precisione estremamente elevata (a livello di micron), con costi relativamente alti. La tecnologia CAD/CAM è ampiamente applicata in questo campo per una personalizzazione efficiente e di alta precisione.
Casting: Utilizzato per realizzare strutture di corone/ponti e protesi. Deve essere eseguita in ambienti sotto vuoto o con gas inerte (argon) per evitare l'ossidazione e l'assorbimento di gas (idrogeno, ossigeno). Le fusioni presentano spesso ritiri, difetti interni e strati di reazione superficiale (α-case), che richiedono un post-trattamento (sabbiatura, mordenzatura acida, pressatura isostatica a caldo - HIP) per migliorare le prestazioni.
Fabbricazione additiva (stampa 3D): Tecniche come la fusione laser selettiva (SLM) e la fusione a fascio elettronico (EBM) consentono di fabbricare parti complesse in titanio (abutment personalizzati, strutture, guide chirurgiche, impianti porosi) direttamente da modelli digitali 3D. Questi metodi offrono un'elevata libertà di progettazione, un uso efficiente dei materiali e la possibilità di creare strutture interne complesse (ad esempio, strutture porose biomimetiche per la crescita dell'osso). Si tratta di una delle principali direzioni di sviluppo futuro (per maggiori dettagli, vedere la sezione 7).
5.2 Tecnologie di modifica della superficie:
La morfologia su micro e nanoscala, la composizione chimica e la bagnabilità (idrofilia) della superficie dell'impianto hanno un impatto decisivo sull'adsorbimento delle proteine, sul comportamento delle cellule (adesione, proliferazione, differenziazione) e sulla velocità e qualità finale dell'osteointegrazione. Le principali tecnologie comprendono:
Trattamenti meccanici:
- Lavorazione/Molatura: Forma superfici lisce o regolarmente strutturate. Utilizzato frequentemente nelle prime applicazioni, oggi si applica principalmente alla regione del collo dell'impianto (per ridurre l'attacco della placca).
- Granigliatura/Sabbiatura: Le superfici vengono bombardate con allumina (Al₂O₃), biossido di titanio (TiO₂) o particelle ceramiche biocompatibili (come l'idrossiapatite, HA) per creare una rugosità macroscopica (su scala micron), aumentando l'area superficiale e la capacità di incastro meccanico. Spesso combinato con la mordenzatura acida.
Trattamenti chimici:
- Acquaforte: Utilizza acidi forti (come HCl/H₂SO₄, HF/HNO₃) per dissolvere la superficie del titanio, formando una complessa morfologia porosa su scala micronica o addirittura nanometrica. Aumenta l'area superficiale specifica e migliora la bagnabilità. Costituisce la base di molti trattamenti compositi.
- Trattamento termico alcalino: Il titanio viene immerso in una soluzione di NaOH e poi riscaldato, formando uno strato di gel di titanato di sodio sulla superficie, che può trasformarsi in apatite simile all'osso nei fluidi corporei, migliorando notevolmente la bioattività.
Trattamenti fisico-chimici:
- Sabbiato, grana grossa, inciso all'acido (SLA®): In primo luogo, la sabbiatura crea una rugosità su scala micrometrica, seguita da una mordenzatura acida per rimuovere i residui della sabbiatura e aggiungere strutture su scala nanometrica. Si tratta attualmente di una delle tecnologie di trattamento superficiale di maggior successo commerciale, ampiamente utilizzate e supportate clinicamente, che accelera significativamente l'osteointegrazione e migliora la stabilità iniziale.
- SLA idrofilo (SLActive®): Dopo il trattamento SLA, le superfici vengono conservate/confezionate sotto protezione di azoto o in soluzione salina per mantenere un'elevata energia superficiale e idrofilia (angolo di contatto vicino a 0°). Idrofilia favorisce notevolmente la rapida diffusione del sangue e dei fluidi corporei sulla superficie dell'impianto, accelerando la formazione della matrice di fibrina e il reclutamento degli osteoblasti, ottenendo una guarigione ossea più rapida (settimane anziché mesi rispetto alla SLA tradizionale).
- Ossidazione anodica: L'applicazione di tensione in un elettrolita consente la crescita controllata di un film di TiO₂ spesso e poroso (che può includere elementi di calcio e fosfato) sulla superficie del titanio. Lo spessore del film (che influisce sull'interferenza cromatica per gli abutment estetici), la porosità e la composizione possono essere controllati con precisione, migliorando la resistenza alla corrosione, la bioattività e (in condizioni specifiche) le proprietà antibatteriche.
Tecnologie di rivestimento:
- Rivestimento in idrossiapatite (HA): Deposito di uno strato ceramico di HA bioattivo su superfici di titanio con metodi quali la spruzzatura al plasma (TPS). È destinato a fornire un'interfaccia diretta osteoconduttiva/osteoinduttiva. Tuttavia, esistono problemi per quanto riguarda l'adesione del rivestimento e la stabilità a lungo termine (possibile degradazione e delaminazione), ed è meno utilizzata della SLA.
- Altri rivestimenti con molecole bioattive: Come le proteine morfogenetiche ossee (BMP), i peptidi (RGD), i fattori di crescita, ecc., attualmente in fase di ricerca, volti a fornire segnali biologici più attivi sulla superficie.
5.3 Effetti dei trattamenti superficiali sulle risposte biologiche e sulle prestazioni cliniche:
- Osseointegrazione accelerata: Le superfici irruvidite (SLA, SLActive) e bioattivate (rivestimento HA, trattamento termico con alcali) riducono significativamente il periodo di guarigione dell'impianto (da 3-6 mesi sulle superfici lisce tradizionali a 3-6 settimane o anche meno), consentendo un carico immediato o precoce e migliorando la soddisfazione del paziente.
- Bloccaggio biomeccanico migliorato: Le superfici ruvide su micro/nanoscala aumentano l'area di contatto osso-impianto (BIC%) e formano strutture meccaniche di interconnessione, migliorando notevolmente la stabilità iniziale dell'impianto e la capacità di carico a lungo termine.
- Impatto sull'attaccamento dei tessuti molli: Le caratteristiche della superficie (come la levigatezza e l'idrofilia) della parte transgengivale (collo) dell'impianto sono cruciali per l'attaccamento delle cellule epiteliali e dei fibroblasti, formando un buon sigillo dei tessuti molli (larghezza biologica), che è fondamentale per prevenire l'invasione batterica e mantenere la salute perimplantare.
- Rischi potenziali: Superfici eccessivamente ruvide o microfessurate possono aumentare il rischio di colonizzazione batterica, richiedendo standard di controllo più elevati per la perimplantite. La stabilità a lungo termine dei rivestimenti (come l'HA) necessita di ulteriori prove.

6. Sfide e limiti
Sebbene il titanio abbia ottenuto un grande successo in odontoiatria, rimangono alcune sfide da affrontare:
6.1 Costi delle materie prime e di lavorazione:
- L'estrazione e la raffinazione dei minerali di titanio (rutilo, ilmenite) attraverso i processi Kroll o Hunter richiedono molta energia e sono complessi e comportano costi delle materie prime notevolmente superiori a quelli dell'acciaio inossidabile o delle leghe di cobalto-cromo.
- La lavorazione del titanio (fusione, lavorazione, stampa 3D) è difficile e richiede attrezzature specializzate, controlli ambientali rigorosi (protezione con gas inerte) e lavoratori altamente qualificati, aumentando ulteriormente i costi di produzione. Ciò rende i prodotti dentali finali a base di titanio (soprattutto impianti e protesi personalizzate) relativamente costosi.
6.2 Allergie o sensibilità rare:
- Il titanio è generalmente considerato estremamente poco allergenico. Tuttavia, casi clinici rari ma documentati riportano un'ipersensibilità di tipo ritardato (reazione allergica di tipo IV) in un numero molto ristretto di individui al metallo titanio o a elementi della lega (ad esempio, alluminio, vanadio, impurità di nichel).
- I sintomi possono includere infiammazione perimplantare persistente, arrossamento e gonfiore della mucosa, dolore e persino fallimento dell'osteointegrazione.
- La diagnosi è difficile a causa della mancanza di test standardizzati altamente specifici e sensibili per l'allergia al titanio (ad esempio, l'interpretazione del patch test è controversa).
- Sebbene l'incidenza sia molto bassa (molto più bassa dell'allergia al nichel), la gestione dei pazienti sospetti (ad esempio, il passaggio a impianti in zirconia) e la ricerca sui meccanismi rimangono argomenti clinici importanti.
6.3 Usura e corrosione elettrochimica in ambienti con metalli misti:
- Fretting/Corrosione: I sistemi implantari comprendono molteplici interfacce metalliche (ad esempio, viti dell'abutment e filettature interne dell'impianto, connessioni abutment-impianto). I micromovimenti funzionali (forze masticatorie, occlusione) causano l'usura da fretting, che danneggia le pellicole di ossido protettivo ed espone il metallo fresco.
- Corrosione galvanica: Quando nella cavità orale sono presenti metalli diversi (ad esempio, impianti in titanio + corone in oro, fili ortodontici in acciaio inossidabile + brackets in titanio) e sono collegati dalla saliva (elettrolita), le differenze di potenziale causano una dissoluzione accelerata della corrosione del metallo con il potenziale più basso (anodo, ad esempio, titanio).
- Anche i diversi gradi o stati superficiali del titanio possono presentare lievi differenze di potenziale.
- Corrosione interstiziale: Nelle connessioni metalliche strettamente aderenti ma non assolutamente sigillate (ad esempio, l'interfaccia moncone-impianto), la ridotta concentrazione di ossigeno, il pH più basso e l'accumulo di ioni cloruro nelle fessure possono indurre una corrosione localizzata.
- Conseguenze: Questi processi di corrosione possono indebolire la resistenza meccanica, rilasciare ioni/particelle metalliche nei tessuti circostanti, innescando eventualmente reazioni locali o sistemiche (ad esempio, allergie, infiammazioni), e compromettere la stabilità e la durata dell'impianto a lungo termine. Un controllo rigoroso della compatibilità dei materiali, un design ottimizzato delle connessioni (ad esempio, guarnizioni coniche Morse) e una migliore precisione di produzione per ridurre i micromovimenti sono le contromisure chiave.
7.Sviluppo e innovazione futuri
Per superare le sfide esistenti e migliorare ulteriormente le prestazioni, la ricerca sui materiali dentali a base di titanio si concentra sulle seguenti direzioni:
7.1 Sviluppo di nuove leghe a base di titanio:
- Ottimizzazione delle leghe senza alluminio e vanadio: Continuare a promuovere e ottimizzare leghe alternative come Ti-6Al-7Nb e sviluppare a fondo leghe di titanio di tipo β con prestazioni superiori e migliore biocompatibilità (ad esempio, leghe del sistema Ti-Nb-Zr-Ta). L'obiettivo è quello di ottenere un modulo elastico ultrabasso vicino al tessuto osseo, limiti di fatica più elevati ed eccellente resistenza alla corrosione.
- Leghe di titanio e zirconio (Ti-Zr): Le leghe rappresentate da Roxolid® (Ti-15Zr) sono state commercializzate con successo. La loro resistenza (>850 MPa) è molto superiore a quella del titanio commercialmente puro (CP) (~550 MPa) e vicina a quella del Ti-6Al-4V (~900 MPa), pur mantenendo una biocompatibilità paragonabile a quella del titanio puro e un'eccellente capacità di osteointegrazione. Le direzioni future includono l'ottimizzazione del contenuto di Zr, l'esplorazione di leghe Ti-Zr combinate con altri elementi (come Nb, Ta) e l'espansione della loro applicazione a una più ampia gamma di componenti di restauro implantare (ad esempio, viti per abutment, abutment personalizzati).
- Leghe a basso modulo e alta resistenza: Progettare leghe con nanostrutture o composizioni di fasi speciali per superare le tradizionali limitazioni di resistenza-modulo delle leghe convenzionali.
7.2 Profonda integrazione della produzione additiva (stampa 3D) e dell'odontoiatria digitale:
- Strutture complesse personalizzate: Le tecnologie SLM/EBM possono produrre con precisione geometrie complesse impossibili con i processi tradizionali, come impianti personalizzati altamente biomimetici, internamente porosi a struttura gradiente (che promuovono la crescita e la vascolarizzazione dell'osso), abutment personalizzati anatomicamente corrispondenti e scaffold per l'aumento dell'osso (Membrane GBR, reti in titanio).
- Ottimizzazione della topologia: Utilizzando algoritmi computerizzati, si progettano strutture implantari o scaffold restaurativi con una distribuzione ottimale del materiale, un peso minimo e una distribuzione delle sollecitazioni più uniforme in base all'analisi delle forze.
- Flusso di lavoro integrato: La stampa 3D si integra perfettamente nei processi di odontoiatria digitale (scansione orale/ acquisizione dati CBCT → progettazione CAD → stampa CAM), ottenendo una produzione completamente tracciabile, efficiente e precisa di restauri/guide implantari/impianti. La riduzione dei costi e il miglioramento dell'accessibilità sono fondamentali per una più ampia adozione.
7.3 Applicazione della nanotecnologia nell'ingegneria della superficie del titanio:
Costruzione di nanostrutture: Attraverso metodi chimici (ad esempio, doppia mordenzatura acida, trattamento alcalino-calorico), fisici (ad esempio, ablazione laser, fascio di ioni) o elettrochimici (ad esempio, anodizzazione), si costruiscono con precisione nanotubi, nanopori, nanoparticelle, nanoregge e altre nanostrutture sulle superfici di titanio. Queste caratteristiche in scala nanometrica imitano più efficacemente la matrice extracellulare (ECM), regolando direttamente il comportamento delle cellule (osteoblasti, cellule staminali), tra cui l'adesione, la diffusione, la migrazione, la proliferazione e la differenziazione, e influenzando persino l'espressione genica.
Rivestimenti nano funzionalizzati:
Rivestimenti antibatterici: Caricare agenti antibatterici come nanoparticelle di argento (AgNPs), nanoparticelle di ossido di zinco (ZnO NPs), peptidi antimicrobici (AMPs), chitosano, ecc. per conferire proprietà antibatteriche di lunga durata alla superficie e prevenire attivamente la perimplantite.
Rivestimenti promotori osteogenici/angiogenici: Caricare fattori di crescita (ad es. BMP-2, VEGF), ioni bioattivi (ad es. Sr²⁺, Mg²⁺, Li⁺) o piccoli farmaci molecolari per regolare con precisione il microambiente locale, promuovendo una rigenerazione ossea e una vascolarizzazione rapide e di alta qualità.
Rivestimenti intelligenti reattivi: Progettare rivestimenti intelligenti che rispondano ai cambiamenti dell'ambiente orale (come l'abbassamento del pH o l'attivazione di enzimi batterici) per rilasciare farmaci antibatterici o antinfiammatori per un trattamento on-demand.
Migliorare la stabilità delle superfici a lungo termine: Studiare la stabilità, il comportamento di degradazione e la risposta biologica delle nanostrutture durante il servizio a lungo termine.
Conclusione
Il titanio e le leghe di titanio si sono affermati nell'odontoiatria moderna, in particolare nell'implantologia dentale, grazie alla loro impareggiabile biocompatibilità, alle eccellenti proprietà meccaniche (in particolare l'elevato rapporto resistenza/peso), all'eccezionale resistenza alla corrosione e alla capacità unica di promuovere l'osteointegrazione. Dagli impianti che servono come radici artificiali dei denti, agli abutment per la connessione e la transizione, alle impalcature di supporto e agli efficienti strumenti ortodontici, i materiali in titanio attraversano tutti gli aspetti del restauro dentale, facendo progredire notevolmente la ricostruzione della funzione orale e il restauro estetico.
Nonostante le sfide poste da costi, allergie rare e corrosione in ambienti a metalli misti, i progressi nella scienza dei materiali e nella tecnologia di produzione continuano ad aprire nuove strade. Le nuove leghe a base di titanio (come le leghe Ti-Zr ad alta resistenza e le leghe di tipo β a basso modulo) mirano a migliorare le prestazioni garantendo al contempo la biosicurezza; la produzione additiva (stampa 3D) ha inaugurato una nuova era di restauri altamente personalizzati e con strutture complesse e la produzione di impianti; l'ingegneria delle superfici nanostrutturate consente una precisione senza precedenti nel controllo dell'interfaccia materiale-biologico, dotando le superfici in titanio di funzioni antibatteriche, osteogeniche e persino di risposta intelligente.
In prospettiva, i materiali a base di titanio rimarranno il "gold standard" e un vettore di innovazione chiave nel restauro degli impianti dentali. Grazie alla continua innovazione dei materiali, ai processi di produzione avanzati e al design preciso delle superfici, l'applicazione del titanio in odontoiatria diventerà sempre più minimamente invasiva, più veloce, più durevole, più personalizzata e più sicura, fornendo ai pazienti soluzioni di restauro orale che eccellono sia nella funzione che nell'estetica, con una prognosi migliore a lungo termine, migliorando significativamente la qualità della vita dei pazienti. La leggendaria storia del titanio nella medicina orale è tutt'altro che conclusa e continua a scrivere nuovi brillanti capitoli.
Riferimenti
Brånemark, P. I., Adell, R., Breine, U., Hansson, B. O., Lindström, J., & Ohlsson, A. (1977). Ancoraggio intraosseo di protesi dentarie. I. Studi sperimentali. Scandinavian Journal of Plastic and Reconstructive Surgery, 11(3), 81-100.
(Ha introdotto il concetto di osteointegrazione e ha stabilito le basi biologiche degli impianti in titanio).
ASTM International. (2019). ASTM F67-13: Specifiche standard per il titanio non legato per applicazioni di impianti chirurgici. ASTM.
ASTM International. (2020). ASTM F136-13: Specifiche standard per la lega ELI di titanio-6alluminio-4vanadio per applicazioni di impianti chirurgici.. ASTM.
(Definisce gli standard di grado medico per il titanio commercialmente puro e la lega Ti-6Al-4V).
Buser, D., Broggini, N., Wieland, M., et al. (2004). Miglioramento dell'apposizione ossea su una superficie di titanio SLA chimicamente modificata. Giornale della ricerca dentale, 83(7), 529-533.
(Studio classico che dimostra l'accelerazione dell'osteointegrazione tramite la modifica della superficie SLA).
Chiapasco, M., Casentini, P., & Zaniboni, M. (2012). Procedure di aumento dell'osso in odontoiatria implantare. Rivista internazionale di impianti orali e maxillo-facciali, 27(Suppl), s183-s203.
(Dati clinici sull'uso della lega Ti-15Zr (Roxolid®) in impianti di diametro ridotto).
Kuroda, D., Niinomi, M., Morinaga, M., et al. (1998). Progettazione e proprietà meccaniche di nuove leghe di titanio di tipo β per materiali da impianto. Scienza e ingegneria dei materiali: A, 243(1-2), 244-249.
(Dimostra i vantaggi biomeccanici delle leghe di titanio di tipo β a basso modulo elastico).
Van Noort, R. (2012). Il futuro dei dispositivi dentali è digitale. Materiali dentali, 28(1), 3-12.
(Esamina le prospettive delle tecnologie di fabbricazione digitale come la stampa 3D per gli impianti dentali).
Mendonça, G., Mendonça, D. B., Aragão, F. J., & Cooper, L. F. (2008). Progressi nella tecnologia delle superfici degli impianti dentali: dal micron alla nanotopografia. Biomateriali, 29(28), 3822-3835.
(Discute di come le topografie di superficie su scala nanometrica modulino il comportamento cellulare).
Siddiqi, A., Payne, A. G., De Silva, R. K., & Duncan, W. J. (2011). Allergia al titanio: Una revisione della letteratura. Rivista internazionale di impianti orali e maxillo-facciali, 26(4), 743-750.
(Revisione sistematica sull'epidemiologia dell'allergia al titanio e sulle sfide diagnostiche).
Reclaru, L. e Meyer, J. M. (1994). La corrosione elettrochimica in odontoiatria restaurativa. Cliniche dentali del Nord America, 38(2), 319-332.
(Esplora i meccanismi di corrosione elettrochimica nell'ambiente orale con più metalli).
Pjetursson, B. E., Thoma, D., Jung, R., et al. (2012). Una revisione sistematica dei tassi di sopravvivenza e di complicanze delle protesi dentali fisse (FDP) supportate da impianti dopo un periodo medio di osservazione di almeno 5 anni. Ricerca clinica sugli impianti orali, 23(Suppl 6), 22-38.
(Fornisce dati basati sull'evidenza sui tassi di sopravvivenza degli impianti nell'arco di 10 anni).