Le titane et ses alliages sont devenus les matériaux de base de la restauration moderne des implants dentaires en raison de leur excellente biocompatibilité, de leurs propriétés mécaniques et de leur capacité d'ostéointégration. Cet article décrit systématiquement la classification des matériaux en titane, leurs principales propriétés, leur large application dans le domaine dentaire (avec les implants comme point central), les technologies de traitement et leur impact, les défis actuels et les perspectives telles que les nouveaux alliages, la fabrication additive et la nano-ingénierie de surface, dans le but de fournir des références théoriques pour la pratique clinique et la recherche.

1. Introduction
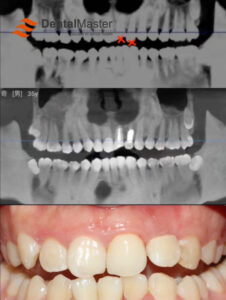
Le titane (Ti), 22e élément du tableau périodique, est un métal de transition blanc argenté. Depuis les années 1950, lorsque le savant suédois Per-Ingvar Brånemark a découvert que le titane pouvait former une connexion directe, fonctionnelle et structurelle avec le tissu osseux (connue sous le nom d'"ostéointégration"), le titane a ouvert un chapitre brillant dans le domaine biomédical, en particulier dans l'implantologie dentaire. Sa combinaison unique de propriétés répond parfaitement aux exigences rigoureuses des matériaux de réhabilitation orale : une excellente biocompatibilité pour éviter le rejet, une résistance spécifique extrêmement élevée pour supporter les forces de mastication, une résistance exceptionnelle à la corrosion contre l'érosion salivaire et une bonne ostéoconductivité pour assurer une stabilité à long terme. Le succès et la prévisibilité des traitements par implants dentaires dépendent fortement de ces caractéristiques fondamentales du titane, ce qui en fait le "roi des biomatériaux" irremplaçable dans les restaurations dentaires, en particulier pour la réhabilitation des dents perdues.
2. Classification du titane et de ses alliages
Les matériaux en titane utilisés dans le domaine dentaire peuvent être classés en deux catégories principales en fonction de leur composition et de leurs propriétés :
- 2.1 Titane commercialement pur (CP Ti) :
- Selon les normes ASTM (par exemple, F67), le CP Ti est divisé en grades 1 à 4 en fonction de la teneur en éléments interstitiels tels que l'oxygène et le fer.
- Caractéristiques : Il présente la meilleure biocompatibilité (le plus inerte), une excellente résistance à la corrosion et une bonne plasticité, ce qui le rend facile à transformer. Toutefois, sa résistance (en particulier sa limite d'élasticité et sa résistance à la fatigue) est relativement faible.
- Applications dentaires : Principalement utilisé pour les implants, les piliers, les armatures de couronnes et de ponts et les brackets orthodontiques lorsque les exigences de résistance ne sont pas extrêmes. Le CP Ti Grade 4 est le plus utilisé.
- 2.2 Alliages de titane :
- L'ajout d'éléments d'alliage (par exemple Al, V, Nb, Zr, Mo, Ta) permet d'améliorer les propriétés mécaniques du titane.
- Alliage représentatif - Ti-6Al-4V (Grade 5) :
- L'alliage classique de titane à phase α+β (6% d'aluminium stabilise la phase α, 4% de vanadium stabilise la phase β).
- Caractéristiques : Beaucoup plus résistant que le CP Ti (environ deux fois la résistance du CP Ti Grade 4), d'excellentes propriétés de fatigue et une bonne résistance à la corrosion. Cependant, la toxicité biologique potentielle du vanadium (V) et de l'aluminium (Al) suscite des inquiétudes (malgré des preuves cliniques limitées), et son module d'élasticité est encore plus élevé que celui de l'os.
- Autres alliages nouveaux/spécifiques aux soins dentaires :
- Ti-6Al-7Nb, Ti-5Al-2,5Fe : Conçu pour remplacer le Ti-6Al-4V, sans vanadium pour une meilleure biocompatibilité.
- Alliages de titane de type β (par exemple, Ti-13Nb-13Zr, Ti-12Mo-6Zr-2Fe - TMZF, Ti-35Nb-7Zr-5Ta) : utilisent le niobium (Nb), le tantale (Ta), le zirconium (Zr) et le molybdène (Mo) comme principaux éléments d'alliage.
- Caractéristiques : Module élastique plus faible (plus proche de l'os, réduisant la protection contre les contraintes), résistance à la fatigue et à la rupture plus élevée, excellente résistance à la corrosion, absence d'éléments controversés (comme le V et l'Al) et biocompatibilité supérieure. Il s'agit là d'un point chaud de la recherche.
- Alliages Ti-Zr (par exemple, Roxolid® - Ti-15Zr) : Développé spécifiquement pour la dentisterie, il offre une résistance plus élevée que le CP Ti et se rapproche de celle du Ti-6Al-4V, mais avec une biocompatibilité plus proche du titane pur et un module d'élasticité modéré. Particulièrement adapté aux implants de petit diamètre.
Tableau 1 : Comparaison des propriétés du titane dentaire commun et des alliages de titane
| Type de matériau | Grade typique | Composition principale | Avantages | Limites | Principales applications dentaires |
|---|---|---|---|---|---|
| Ti commercialement pur | Première année | >99% Ti | Meilleure biocompatibilité, excellente résistance à la corrosion, ductile | Résistance la plus faible | Parties à parois minces, membranes |
| Niveau 2 | >98,9% Ti | Bonne performance globale (équilibre entre biocompatibilité, résistance à la corrosion, solidité, plasticité) | Résistance modérée | Piliers, petites restaurations, brackets | |
| Niveau 3 | >98,8% Ti | Résistance supérieure à celle du grade 2 | Légèrement moins ductile que le grade 2 | Implants (certains), piliers, armatures | |
| Grade 4 | >98,6% Ti | CP Ti le plus fort | Ductilité inférieure à celle du CP Ti de qualité inférieure | Implants, piliers et fils d'arcs courants | |
| α+β Alliages de titane | Ti-6Al-4V (Gr5) | Ti-6Al-4V | Haute résistance, excellente résistance à la fatigue | Contient de l'Al/V (bio-toxicité potentielle), module d'élasticité élevé | Implants dans les zones à forte charge, connecteurs, outils chirurgicaux |
| Ti-6Al-7Nb | Ti-6Al-7Nb | Résistance proche de Gr5, pas de V (meilleure biocompatibilité) | Contient de l'Al | Implants (substitut Gr5) | |
| Alliages de type β | Ti-13Nb-13Zr | Ti-13Nb-13Zr | Faible module d'élasticité, excellente biocompatibilité, pas d'Al/V | Traitement complexe | Implants (pour atténuer le stress shielding), fils orthodontiques |
| Ti-12Mo-6Zr-2Fe (TMZF) | Ti-12Mo-6Zr-2Fe | Faible module d'élasticité, haute résistance, bonne résistance à la corrosion | Contient du Fe (données biologiques limitées à long terme) | Implants, implants orthopédiques | |
| Alliage spécifique pour les soins dentaires | Ti-15Zr (Roxolid®) | Ti-15Zr | Beaucoup plus résistant que CP4, proche de Gr5, biocompatibilité proche de CP Ti | Coût plus élevé | Implants de petit diamètre/à crête étroite |
(Remarque : ce tableau est une comparaison simplifiée. Les paramètres de performance exacts doivent être indiqués dans les normes relatives aux matériaux et dans les données du fabricant. Module d'élasticité : CP Ti ~100-110 GPa, Ti-6Al-4V ~110-115 GPa, alliages β ~55-85 GPa, os cortical ~10-30 GPa)
3. Principaux avantages du titane en dentisterie
Le titane et ses alliages présentent des avantages inégalés dans les applications dentaires :
- 3.1 Biocompatibilité et résistance à la corrosion exceptionnelles :
- Biocompatibilité : Le titane peut former spontanément un film passif dense, stable et inerte de dioxyde de titane (TiO₂) dans des environnements physiologiques. Ce film isole efficacement la libération d'ions métalliques dans les tissus environnants, minimisant l'inflammation et le rejet immunitaire - une condition préalable à l'ostéointégration. De nombreuses études cliniques et données de suivi à long terme confirment l'excellente réponse tissulaire des implants en titane.
- Résistance à la corrosion : La couche passive de TiO₂ présente une forte résistance aux fluides corporels (salive, sang, liquide interstitiel), aux fluorures (provenant du dentifrice et du bain de bouche) et aux fluctuations du pH buccal (provenant par exemple d'aliments et de boissons acides). Même au cours d'une utilisation à long terme, les problèmes tels que les piqûres, la corrosion caverneuse ou la fissuration par corrosion sous contrainte sont extrêmement rares, ce qui garantit la stabilité chimique à long terme et la sécurité des implants dans l'environnement buccal difficile.
- 3.2 Rapport résistance/poids élevé (résistance spécifique élevée) :
Le titane a une densité nettement inférieure (~4,5 g/cm³) à celle de l'acier inoxydable (~8 g/cm³) et des alliages cobalt-chrome (~8,5 g/cm³), mais sa résistance (en particulier celle des alliages de titane) est comparable, voire supérieure, à celle de ces matériaux. Cela signifie que les restaurations ou les implants en titane peuvent offrir une capacité de charge suffisante (résister aux forces de mastication, généralement jusqu'à plusieurs centaines de newtons) tout en étant plus légers, réduisant ainsi la charge sur les tissus de soutien et améliorant le confort du patient. - 3.3 Excellente capacité d'ostéointégration :
C'est l'avantage principal du titane en tant que matériau d'implant. La couche de TiO₂ à la surface du titane est bioactive et peut adsorber sélectivement les protéines du sang et des fluides corporels (comme le fibrinogène et la fibronectine), favorisant l'adhésion, la prolifération et la différenciation des ostéoblastes. Finalement, le nouveau tissu osseux peut se déposer directement et se lier étroitement à la surface du titane, formant une connexion structurelle et fonctionnelle directe sans interface de tissu conjonctif fibreux. Cette intégration directe de l'os à l'implant constitue la base biologique de la rétention stable à long terme de l'implant. - 3.4 Radiolucidité et avantages esthétiques :
Radiolucidité : Le titane présente une atténuation des rayons X beaucoup plus faible que les métaux traditionnels tels que les alliages d'or et les alliages cobalt-chrome. Sur les radiographies (films périapicaux, films panoramiques, CBCT), les implants en titane apparaissent comme des images relativement peu denses, permettant une visualisation claire de la structure osseuse environnante. Cela facilite l'évaluation précise par les cliniciens de l'état d'ostéointégration, des changements du niveau de l'os marginal et de la santé péri-implantaire, ce qui en fait un élément clé pour le suivi à long terme.
Avantage esthétique : Dans le cas d'une gencive fine ou d'implants placés superficiellement (en particulier dans la zone antérieure), les piliers métalliques traditionnels (par exemple, les alliages d'or) peuvent provoquer une décoloration grisâtre à travers la gencive, ce qui nuit à l'esthétique. Bien que les piliers en titane puissent présenter un risque similaire, leur teinte grise est généralement plus claire et peut être complètement évitée en choisissant des piliers entièrement en céramique ou des piliers en titane avec des revêtements en céramique ou en zircone. En tant que matériau pour les piliers ou les armatures, le titane fournit également un support fiable pour les restaurations tout-céramique, ce qui permet d'obtenir des résultats esthétiques d'apparence naturelle.

4. Applications courantes du titane en dentisterie
Le titane est largement utilisé dans divers domaines de la restauration dentaire, de l'implantation, de l'orthodontie et de la chirurgie :
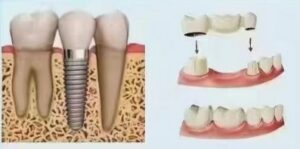
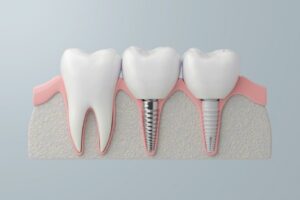
4.1 Implants dentaires :
Il s'agit de l'application la plus centrale et la plus réussie du titane en dentisterie. Implants en titane servent de racines dentaires artificielles, insérées chirurgicalement dans l'os de la mâchoire pour soutenir des superstructures (couronnes, ponts, prothèses). Leurs conceptions (forme de racine, cylindrique, forme de lame), leurs traitements de surface (SLA, SLActive, anodisation, etc.) et leurs méthodes de connexion (hexagone interne, cône Morse, commutation de plate-forme) continuent d'évoluer pour répondre aux différentes conditions osseuses, aux besoins prothétiques et aux exigences esthétiques. Le taux de réussite à long terme (plus de 10 ans) dépasse souvent 95% dans le cadre d'indications strictes.
4.2 Piliers et composants prothétiques :
Piliers : Les composants clés qui relient la plate-forme de l'implant à la superstructure. Ils peuvent être en titane (CP Ti ou alliage), en zircone ou une combinaison (base en titane + sommet en zircone). Piliers en titane sont robustes, fiables en liaison avec les implants et biocompatibles, ce qui en fait un choix courant, particulièrement adapté aux régions postérieures ou aux piliers angulaires.
Vis prothétiques : Utilisés pour fixer les piliers ou les restaurations aux implants, ils sont généralement fabriqués à partir d'alliages de titane à haute résistance (par exemple, Ti-6Al-4V). Ils nécessitent une résistance à la fatigue et une précision dimensionnelle extrêmement élevées.
Manchons, Connecteurs : Dans les structures prothétiques complexes (telles que les prothèses adjointes sur barre), les connecteurs en titane assurent la stabilité et la solidité.
4.3 Arcs et brackets orthodontiques :
Fils d'arcs : Les alliages de titane bêta (par exemple, TMA - alliage de titane et de molybdène) sont privilégiés en orthodontie fixe en raison de leur module d'élasticité inférieur (forces plus souples et continues), de leur limite d'élasticité élevée (grande plage de déformation), de leur bonne aptitude à la déformation et de leur biocompatibilité. Ils sont couramment utilisés aux stades ultérieurs pour les ajustements fins.
Supports : Les brackets métalliques en titane sont principalement utilisés pour les patients allergiques au nickel, car ils offrent une bonne biocompatibilité et une résistance suffisante.
4.4 Outils et instruments chirurgicaux :
L'excellente solidité, la légèreté et la résistance à la corrosion du titane en font un matériau idéal pour la fabrication de produits de haute précision et durables. instruments de chirurgie dentaireCes produits sont utilisés dans des domaines tels que les guides chirurgicaux pour implants, les ostéotomes, les porte-aiguilles, les rétracteurs et les porte-implants/clé à molette. Sa nature non magnétique convient également aux environnements d'examen spéciaux (par exemple, l'IRM).
4.5 Couronnes, bridges et armatures (armatures pour prothèses dentaires) :
Cadres de la Couronne/Ponts : Le titane commercialement pur (principalement les grades 1 et 2) peut être coulé ou fraisé par CAO/FAO pour fabriquer des couronnes ou des bridges. Les avantages sont la légèreté, la bonne biocompatibilité et la radiotransparence. Les inconvénients sont les difficultés de coulée (oxydation, rétraction) et une esthétique inférieure à celle du tout-céramique (la porcelaine de recouvrement est nécessaire et la liaison avec le titane est un défi majeur).
Armatures de prothèses amovibles : Par rapport aux alliages traditionnels de cobalt et de chrome, les armatures en titane réduisent considérablement le poids, améliorent le confort de port, renforcent la biocompatibilité, ont moins d'impact sur le goût et ne posent pas de problèmes d'allergie. Elles sont couramment utilisées dans les bases et les crochets des prothèses amovibles partielles.

5. Traitement du titane et traitement de surface : La clé des performances de façonnage
Les performances du titane dépendent non seulement de ses propriétés intrinsèques, mais aussi fortement de ses méthodes de traitement et de l'état de sa surface, ce qui est particulièrement crucial pour l'ostéointégration de l'implant.
5.1 Techniques de traitement :
Travail à froid : Comme le laminage et l'étirage, utilisés pour produire des fils de titane (arcs orthodontiques), des feuilles (armatures) et des tiges (piliers usinés), ébauches d'implants). Augmente la résistance mais réduit la ductilité.
Usinage (fabrication soustractive) : Principale méthode de fabrication d'implants, de piliers et de composants prothétiques personnalisés. Elle nécessite des machines à haute rigidité, des outils spécialisés (en carbure, revêtus de diamant) et un liquide de refroidissement (empêchant strictement l'oxydation). Une précision extrêmement élevée est nécessaire (de l'ordre du micron), avec des coûts relativement élevés. La technologie CAD/CAM est largement appliquée dans ce domaine pour une personnalisation efficace et de haute précision.
Casting : Utilisé pour fabriquer des armatures de couronnes et de bridges et des structures de prothèses dentaires. Le travail doit être effectué sous vide ou sous gaz inerte (argon) afin d'éviter l'oxydation et l'absorption de gaz (hydrogène, oxygène). Les pièces coulées présentent souvent un retrait, des défauts internes et des couches de réaction superficielle (α-case), ce qui nécessite un post-traitement (sablage, décapage à l'acide, pressage isostatique à chaud - HIP) pour améliorer les performances.
Fabrication additive (impression 3D) : Des techniques telles que la fusion sélective au laser (SLM) et la fusion par faisceau d'électrons (EBM) permettent de fabriquer des pièces complexes en titane (piliers personnalisés, armatures, guides chirurgicaux, implants poreux) directement à partir de modèles numériques en 3D. Ces méthodes offrent une grande liberté de conception, une utilisation efficace des matériaux et la possibilité de créer des structures internes complexes (par exemple, des structures poreuses biomimétiques pour la croissance osseuse). Il s'agit de l'une des principales orientations du développement futur (voir la section 7 pour plus de détails).
5.2 Technologies de modification de la surface :
La morphologie micro- et nanométrique, la composition chimique et la mouillabilité (hydrophilie) de la surface de l'implant ont un impact décisif sur l'adsorption des protéines, le comportement des cellules (adhésion, prolifération, différenciation) et la vitesse et la qualité finales de l'ostéo-intégration. Les principales technologies sont les suivantes :
Traitements mécaniques :
- Usinage et broyage : Forme des surfaces lisses ou régulièrement texturées. Utilisé fréquemment dans les premières applications, il est aujourd'hui principalement appliqué à la région du col de l'implant (pour réduire l'attachement de la plaque).
- Sablage et grenaillage : Les surfaces sont bombardées d'alumine (Al₂O₃), de dioxyde de titane (TiO₂) ou de particules céramiques biocompatibles (telles que l'hydroxyapatite, HA) pour créer une rugosité macroscopique (à l'échelle du micron), augmentant ainsi la surface et la capacité d'imbrication mécanique. Souvent combiné avec une attaque à l'acide.
Traitements chimiques :
- Gravure à l'acide : Utilise des acides forts (tels que les mélanges HCl/H₂SO₄, HF/HNO₃) pour dissoudre la surface du titane, formant une morphologie poreuse complexe à l'échelle du micron ou même du nanomètre. Augmente la surface spécifique et améliore la mouillabilité. Constitue la base de nombreux traitements composites.
- Traitement thermique alcalin : Le titane est immergé dans une solution de NaOH puis chauffé, ce qui forme une couche de gel de titanate de sodium à la surface, qui peut se transformer en apatite semblable à l'os dans les fluides corporels, ce qui améliore considérablement la bioactivité.
Traitements physico-chimiques :
- Sablage, gros grain, gravure à l'acide (SLA®) : Tout d'abord, le sablage crée une rugosité à l'échelle du micron, suivi d'une attaque à l'acide pour éliminer les résidus de sablage et ajouter des structures à l'échelle nanométrique. Il s'agit actuellement de l'une des technologies de traitement de surface les plus réussies sur le plan commercial, les plus largement utilisées et les mieux étayées sur le plan clinique, qui accélère considérablement l'ostéointégration et améliore la stabilité initiale.
- SLA hydrophile (SLActive®) : Après le traitement SLA, les surfaces sont stockées/emballées sous protection d'azote ou dans une solution saline pour maintenir une énergie de surface élevée et une hydrophilie (angle de contact proche de 0°). Hydrophilie favorise grandement l'étalement rapide du sang et des fluides corporels sur la surface de l'implant, accélérant la formation de la matrice de fibrine et le recrutement des ostéoblastes, ce qui permet une cicatrisation osseuse plus rapide (quelques semaines au lieu de plusieurs mois par rapport à la méthode SLA traditionnelle).
- Oxydation anodique : L'application d'une tension dans un électrolyte permet la croissance contrôlée d'un film épais et poreux de TiO₂ (qui peut comprendre des éléments de calcium et de phosphate) sur la surface du titane. L'épaisseur du film (qui affecte l'interférence des couleurs pour les piliers esthétiques), la porosité et la composition peuvent être contrôlées avec précision, ce qui améliore la résistance à la corrosion, la bioactivité et (dans des conditions spécifiques) les propriétés antibactériennes.
Technologies de revêtement :
- Revêtement d'hydroxyapatite (HA) : Dépôt d'une couche de céramique HA bioactive sur des surfaces en titane par des méthodes telles que la pulvérisation de plasma (TPS). L'objectif est de créer une interface ostéoconductrice/ostéoinductrice directe. Cependant, il existe des problèmes concernant l'adhérence du revêtement et la stabilité à long terme (dégradation et délamination possibles), et cette méthode est moins utilisée que la SLA.
- Autres revêtements à base de molécules bioactives : Comme les protéines morphogénétiques osseuses (BMP), les peptides (RGD), les facteurs de croissance, etc.
5.3 Effets des traitements de surface sur les réponses biologiques et la performance clinique :
- Osséointégration accélérée : Les surfaces rugueuses (SLA, SLActive) et bioactivées (revêtement HA, traitement thermique alcalin) raccourcissent considérablement la période de cicatrisation de l'implant (de 3 à 6 mois sur les surfaces lisses traditionnelles à 3 à 6 semaines, voire moins), ce qui permet une mise en charge immédiate ou précoce et améliore la satisfaction du patient.
- Verrouillage biomécanique amélioré : Les surfaces rugueuses à l'échelle micro/nanométrique augmentent la zone de contact entre l'os et l'implant (BIC%) et forment des structures d'emboîtement mécanique, ce qui améliore considérablement la stabilité initiale de l'implant et la capacité de charge à long terme.
- Impact sur l'attachement des tissus mous : Les caractéristiques de surface (telles que la douceur et l'hydrophilie) de la partie transgingivale (col) de l'implant sont cruciales pour l'attachement des cellules épithéliales et des fibroblastes, formant un bon joint de tissu mou (largeur biologique), ce qui est essentiel pour prévenir l'invasion bactérienne et maintenir la santé péri-implantaire.
- Risques potentiels : Les surfaces excessivement rugueuses ou microfissurées peuvent augmenter le risque de colonisation bactérienne, ce qui nécessite des normes de contrôle plus strictes pour la péri-implantite. La stabilité à long terme des revêtements (tels que l'AH) doit encore être démontrée.

6. Défis et limites
Bien que le titane ait connu un grand succès en dentisterie, certains défis restent à relever :
6.1 Coûts des matières premières et de la transformation :
- L'extraction et le raffinage des minerais de titane (rutile, ilménite) par les procédés Kroll ou Hunter sont énergivores et complexes, ce qui se traduit par des coûts de matières premières nettement supérieurs à ceux de l'acier inoxydable ou des alliages de cobalt-chrome.
- La transformation du titane (moulage, usinage, impression 3D) est difficile et nécessite des équipements spécialisés, des contrôles environnementaux stricts (protection par gaz inerte) et des travailleurs hautement qualifiés, ce qui augmente encore les coûts de fabrication. Cela rend les produits dentaires finaux à base de titane (en particulier les implants et les restaurations personnalisées) relativement coûteux.
6.2 Allergies ou sensibilités rares :
- Le titane est généralement considéré comme extrêmement peu allergène. Cependant, des cas cliniques rares mais documentés font état d'une hypersensibilité retardée (réaction allergique de type IV) chez un très petit nombre d'individus au métal titane ou à des éléments d'alliage (par exemple, aluminium, vanadium, impuretés de nickel).
- Les symptômes peuvent inclure une inflammation péri-implantaire persistante, une rougeur et un gonflement de la muqueuse, une douleur, voire un échec de l'ostéo-intégration.
- Le diagnostic est difficile à établir en raison du manque de tests standardisés d'allergie au titane hautement spécifiques et sensibles (par exemple, l'interprétation des tests épicutanés est controversée).
- Bien que l'incidence soit très faible (beaucoup moins que l'allergie au nickel), la prise en charge des patients suspects (par exemple, le passage à des implants en zircone) et la recherche sur les mécanismes restent des sujets cliniques importants.
6.3 Usure et corrosion électrochimique dans les environnements métalliques mixtes :
- Fretting/Corrosion : Les systèmes implantaires comportent de multiples interfaces métalliques (par exemple, vis de pilier et filets internes de l'implant, connexions pilier-implant). Les micro-mouvements fonctionnels (forces de mastication, occlusion) provoquent une usure de contact qui endommage les films d'oxyde protecteurs et expose le métal frais.
- Corrosion galvanique : Lorsque différents métaux sont présents dans la cavité buccale (par exemple, implants en titane + couronnes en or, fils orthodontiques en acier inoxydable + brackets en titane) et sont reliés par la salive (électrolyte), les différences de potentiel provoquent une dissolution accélérée par corrosion du métal au potentiel le plus faible (anode, par exemple, le titane).
- Même les différentes qualités ou états de surface du titane peuvent présenter de légères différences potentielles.
- Corrosion par crevasses : Dans les connexions métalliques étroitement ajustées mais non absolument étanches (par exemple, l'interface pilier-implant), une concentration réduite en oxygène, un pH plus faible et l'accumulation d'ions chlorure dans les crevasses peuvent induire une corrosion localisée.
- Conséquences : Ces processus de corrosion peuvent affaiblir la résistance mécanique, libérer des ions/particules métalliques dans les tissus environnants, déclenchant éventuellement des réactions locales ou systémiques (par exemple, allergie, inflammation), et affecter la stabilité et la durée de vie à long terme de l'implant. Un contrôle strict de la compatibilité des matériaux, des conceptions de connexion optimisées (par exemple, des joints à cône morse) et une précision de fabrication améliorée pour réduire les micromouvements sont des contre-mesures essentielles.
7. le développement futur et l'innovation
Pour surmonter les difficultés existantes et améliorer encore les performances, la recherche sur les matériaux dentaires à base de titane se concentre sur les orientations suivantes :
7.1 Développement de nouveaux alliages à base de titane :
- Optimisation des alliages sans aluminium ni vanadium : Continuer à promouvoir et à optimiser les alliages alternatifs tels que le Ti-6Al-7Nb, et développer en profondeur les alliages de titane de type β avec des performances supérieures et une meilleure biocompatibilité (par exemple, les alliages du système Ti-Nb-Zr-Ta). L'objectif est d'obtenir un module d'élasticité ultra-faible proche du tissu osseux, des limites de fatigue plus élevées et une excellente résistance à la corrosion.
- Alliages de titane et de zirconium (Ti-Zr) : Les alliages représentés par Roxolid® (Ti-15Zr) ont été commercialisés avec succès. Leur résistance (>850 MPa) est beaucoup plus élevée que celle du titane commercialement pur (CP) (~550 MPa) et proche de celle du Ti-6Al-4V (~900 MPa), tout en conservant une biocompatibilité comparable à celle du titane pur et une excellente capacité d'ostéo-intégration. Les orientations futures comprennent l'optimisation de la teneur en Zr, l'exploration des alliages Ti-Zr combinés à d'autres éléments (tels que Nb, Ta) et l'extension de leur application à une gamme plus large de composants de restauration d'implants (par exemple, vis de pilier, piliers personnalisés).
- Alliages à faible module et à haute résistance : Concevoir des alliages avec des nanostructures ou des compositions de phases spéciales pour dépasser les limites traditionnelles de résistance et de module des alliages conventionnels.
7.2 Intégration profonde de la fabrication additive (impression 3D) et de la dentisterie numérique :
- Structures complexes personnalisées : Les technologies SLM/EBM peuvent fabriquer avec précision des géométries complexes impossibles à réaliser avec les procédés traditionnels, comme des implants personnalisés à structure en gradient hautement biomimétique et à porosité interne (favorisant la croissance osseuse et la vascularisation), des piliers personnalisés adaptés à l'anatomie et des échafaudages d'augmentation osseuse (Membranes GBR, mailles en titane).
- Optimisation de la topologie : À l'aide d'algorithmes informatiques, concevoir des structures d'implants ou d'échafaudages de restauration avec une distribution optimale des matériaux, un poids minimal et une distribution des contraintes la plus uniforme possible, sur la base d'une analyse des forces.
- Flux de travail intégré : L'impression 3D s'intègre de manière transparente dans les processus de dentisterie numérique (numérisation orale/acquisition de données CBCT → conception CAO → impression FAO), ce qui permet une fabrication entièrement traçable, efficace et précise des restaurations/guides d'implants/implants. La réduction des coûts et l'amélioration de l'accessibilité sont les clés d'une adoption plus large.
7.3 Application de la nanotechnologie à l'ingénierie de surface du titane :
Construction de la nanostructure : Grâce à des méthodes chimiques (par exemple, double attaque acide, traitement alcalino-thermique), physiques (par exemple, ablation laser, faisceau d'ions) ou électrochimiques (par exemple, anodisation), des nanotubes, des nanopores, des nanoparticules, des nano-rides et d'autres nanostructures sont construits avec précision sur les surfaces de titane. Ces caractéristiques nanométriques imitent plus efficacement la matrice extracellulaire (ECM), régulant directement le comportement des cellules (ostéoblastes, cellules souches), notamment l'adhésion, l'étalement, la migration, la prolifération et la différenciation, et influençant même l'expression des gènes.
Nano revêtements fonctionnalisés :
Revêtements antibactériens : Charger des agents antibactériens tels que des nanoparticules d'argent (AgNPs), des nanoparticules d'oxyde de zinc (ZnO NPs), des peptides antimicrobiens (AMPs), du chitosan, etc., pour conférer des propriétés antibactériennes durables à la surface et prévenir activement la péri-implantite.
Revêtements favorisant l'ostéogénèse et l'angiogénèse : Charger des facteurs de croissance (par exemple, BMP-2, VEGF), des ions bioactifs (par exemple, Sr²⁺, Mg²⁺, Li⁺), ou des médicaments à petites molécules pour réguler précisément le microenvironnement local, favorisant une régénération osseuse et une vascularisation rapides et de haute qualité.
Revêtements réactifs intelligents : Concevoir des revêtements intelligents qui réagissent aux changements de l'environnement buccal (tels que la baisse du pH ou l'activation d'une enzyme bactérienne) pour libérer des médicaments antibactériens ou anti-inflammatoires en vue d'un traitement à la demande.
Améliorer la stabilité à long terme des surfaces : Étudier la stabilité, le comportement de dégradation et la réponse biologique des nanostructures au cours de leur utilisation à long terme.
Conclusion
Le titane et les alliages de titane se sont imposés dans la dentisterie moderne, en particulier dans l'implantologie dentaire, en raison de leur biocompatibilité inégalée, de leurs excellentes propriétés mécaniques (rapport résistance/poids particulièrement élevé), de leur résistance exceptionnelle à la corrosion et de leur capacité unique à favoriser l'ostéo-intégration. Qu'il s'agisse d'implants servant de racines dentaires artificielles, de piliers de connexion et de transition, d'échafaudages de soutien ou d'outils orthodontiques efficaces, les matériaux en titane sont présents dans tous les aspects de la restauration dentaire, faisant grandement progresser la reconstruction de la fonction buccale et la restauration esthétique.
En dépit de difficultés telles que le coût, les allergies rares et la corrosion dans les environnements mixtes, les progrès de la science des matériaux et de la technologie de fabrication continuent d'ouvrir de nouvelles voies. De nouveaux alliages à base de titane (tels que les alliages Ti-Zr à haute résistance et les alliages de type β à faible module) visent à améliorer les performances tout en garantissant la biosécurité ; la fabrication additive (impression 3D) a ouvert une nouvelle ère de restaurations et de fabrication d'implants hautement personnalisés et à structure complexe ; et l'ingénierie des surfaces nanostructurées permet une précision sans précédent dans le contrôle de l'interface matériau-biologie, dotant les surfaces de titane de fonctions antibactériennes, ostéogéniques, et même de fonctions réactives intelligentes.
À l'avenir, les matériaux à base de titane resteront l'"étalon-or" et un vecteur d'innovation clé dans la restauration des implants dentaires. Grâce à l'innovation continue des matériaux, aux processus de fabrication avancés et à la conception précise des surfaces, l'application du titane en dentisterie évoluera vers une invasivité minimale, plus rapide, plus durable, plus personnalisée et plus sûre, offrant finalement aux patients des solutions de restauration orale qui excellent à la fois en termes de fonction et d'esthétique, avec un meilleur pronostic à long terme, améliorant ainsi de manière significative la qualité de vie des patients. L'histoire légendaire du titane dans la médecine bucco-dentaire est loin d'être terminée et continue d'écrire de nouveaux chapitres brillants.
Références
Brånemark, P. I., Adell, R., Breine, U., Hansson, B. O., Lindström, J. et Ohlsson, A. (1977). Ancrage intra-osseux des prothèses dentaires. I. Études expérimentales. Journal scandinave de chirurgie plastique et reconstructive, 11(3), 81-100.
(A introduit le concept d'ostéointégration et a établi le fondement biologique des implants en titane).
ASTM International. (2019). ASTM F67-13 : Spécification standard pour le titane non allié destiné aux implants chirurgicaux. ASTM.
ASTM International. (2020). ASTM F136-13 : Spécification standard pour l'alliage ELI corroyé de titane-6aluminium-4vanadium pour les applications d'implants chirurgicaux. ASTM.
(Définit les normes de qualité médicale pour le titane commercialement pur et l'alliage Ti-6Al-4V).
Buser, D., Broggini, N., Wieland, M., et al. (2004). Enhanced bone apposition to a chemically modified SLA titanium surface (Apposition osseuse améliorée à une surface de titane SLA chimiquement modifiée). Journal de la recherche dentaire, 83(7), 529-533.
(Étude classique démontrant l'accélération de l'ostéointégration par la modification de la surface SLA).
Chiapasco, M., Casentini, P. et Zaniboni, M. (2012). Procédures d'augmentation osseuse en dentisterie implantaire. International Journal of Oral & Maxillofacial Implants, 27(Suppl), s183-s203.
(Données cliniques sur l'utilisation de l'alliage Ti-15Zr (Roxolid®) dans les implants à diamètre étroit).
Kuroda, D., Niinomi, M., Morinaga, M., et al. (1998). Conception et propriétés mécaniques de nouveaux alliages de titane de type β pour les matériaux d'implant. Science et génie des matériaux : A, 243(1-2), 244-249.
(Démontre les avantages biomécaniques des alliages de titane de type β à faible module d'élasticité).
Van Noort, R. (2012). L'avenir des appareils dentaires est numérique. Matériaux dentaires, 28(1), 3-12.
(Examine les perspectives des technologies de fabrication numérique telles que l'impression 3D pour les implants dentaires).
Mendonça, G., Mendonça, D. B., Aragão, F. J. et Cooper, L. F. (2008). Faire progresser la technologie de surface des implants dentaires : du micron à la nanotopographie. Biomatériaux, 29(28), 3822-3835.
(Explique comment les topographies de surface à l'échelle nanométrique modulent le comportement cellulaire.)
Siddiqi, A., Payne, A. G., De Silva, R. K. et Duncan, W. J. (2011). Titanium allergy : A literature review. International Journal of Oral & Maxillofacial Implants, 26(4), 743-750.
(Revue systématique sur l'épidémiologie de l'allergie au titane et les défis diagnostiques).
Reclaru, L. et Meyer, J. M. (1994). Electrochemical corrosion in restorative dentistry. Cliniques dentaires d'Amérique du Nord, 38(2), 319-332.
(Exploration des mécanismes de corrosion électrochimique dans l'environnement buccal avec plusieurs métaux).
Pjetursson, B. E., Thoma, D., Jung, R., et al. (2012). Une revue systématique des taux de survie et de complications des prothèses dentaires fixes implanto-portées (FDP) après une période d'observation moyenne d'au moins 5 ans. Recherche clinique sur les implants oraux, 23(Suppl 6), 22-38.
(Fournit des données factuelles sur les taux de survie des implants sur 10 ans).